题目内容
用下列实验装置完成对应的实验,无明显错误或不足的是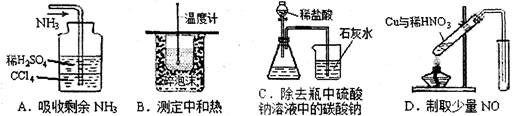

A
本题考查化学实验知识,关键明确各种实验装置的用途。A项中氨气通过CCl4后再被稀硫酸吸不会引起倒吸,A正确;B项中少了环形玻璃搅拌棒,不正确;C项中易发生倒吸,C错;NO不能排气收集,被氧化为NO2,不正确。

练习册系列答案
 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目
题目内容


 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案