题目内容
(14分)实验室用燃烧法测定某固体有机物A的分子组成,测定装置如图(铁架台、铁夹、酒精灯等未画出):

取17.1 g A放入装置中,通入过量O2燃烧,生成CO2和H2O,请回答下列有关问题:
(1)通入过量O2的目的是______________________________________________。
(2)C装置的作用是__________________________________________;
D装置的作用是_____________________________________________。
(3)通过该实验,能否确定A中是否含有氧原子?________。
(4)若A的摩尔质量为342 g/mol,C装置增重9.99 g,D装置增重26.4 g,则A分子式为____________。
(5)写出A燃烧的化学方程式_____________________________________。
(6)A可发生水解反应,1 mol A可水解生成2 mol同分异构体,则A在催化剂作用下水解的化学方程式为_________________________________________。

取17.1 g A放入装置中,通入过量O2燃烧,生成CO2和H2O,请回答下列有关问题:
(1)通入过量O2的目的是______________________________________________。
(2)C装置的作用是__________________________________________;
D装置的作用是_____________________________________________。
(3)通过该实验,能否确定A中是否含有氧原子?________。
(4)若A的摩尔质量为342 g/mol,C装置增重9.99 g,D装置增重26.4 g,则A分子式为____________。
(5)写出A燃烧的化学方程式_____________________________________。
(6)A可发生水解反应,1 mol A可水解生成2 mol同分异构体,则A在催化剂作用下水解的化学方程式为_________________________________________。
(1)使有机物A充分燃烧
(2)吸收A燃烧后生成的H2O 吸收A燃烧后生成的CO2
(3)能 (4)C12H22O11
(5)C12H22O11+12O2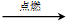 12CO2+11H2O
12CO2+11H2O
(6)C12H22O11(蔗糖)+H2O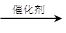 C6H12O6(葡萄糖)+C6H12O6(果糖)
C6H12O6(葡萄糖)+C6H12O6(果糖)
(2)吸收A燃烧后生成的H2O 吸收A燃烧后生成的CO2
(3)能 (4)C12H22O11
(5)C12H22O11+12O2
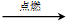 12CO2+11H2O
12CO2+11H2O(6)C12H22O11(蔗糖)+H2O
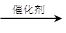 C6H12O6(葡萄糖)+C6H12O6(果糖)
C6H12O6(葡萄糖)+C6H12O6(果糖)试题分析:(1)通入过量O2可以使有机物A充分燃烧,防止生成CO。
(2)浓硫酸具有吸水性,所以C装置的作用是吸收A燃烧后生成的H2O;碱石灰可以吸收CO2,所以D装置的主要作用是吸收A燃烧后生成的CO2。
(3)根据原子守恒可知和质量守恒定律可以判断出有机物中是否含有氧原子。
(4)根据题意A的物质的量是17.1g÷342 g/mol=0.05mol。水蒸气的物质的量是9.99g÷18g/mol=0.55mol,CO2的物质的量是26.4g÷44gmol=0.6mol。所以有机物中含有的碳、氢原子数目分别是0.6÷0.05=12、0.55×2÷0.05=22。所以含有的氧原子数目是
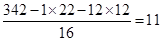 ,即A的分子式是C12H22O11。
,即A的分子式是C12H22O11。(5)A燃烧的生成物是水和CO2,所以燃烧的化学方程式是C12H22O11+12O2
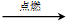 12CO2+11H2O。
12CO2+11H2O。(6)1 mol A可水解生成2 mol同分异构体,则根据A的分子式可知,A是蔗糖,水解生成葡萄糖和果糖,化学方程式是C12H22O11(蔗糖)+H2O
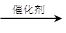 C6H12O6(葡萄糖)+C6H12O6(果糖)。
C6H12O6(葡萄糖)+C6H12O6(果糖)。点评:在根据有机物燃烧的有关计算,特别是在判断是否含有氧原子时,需要依据原子守恒和质量守恒定律等进行列式解答,。其次还需要搞清楚哪些试剂是吸水的,哪些试剂是吸收CO2的。

练习册系列答案
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案
相关题目



