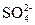题目内容
在标准状况下,SO2和O2混合气体500 mL,通过灼热V2O5层后,体积变为450 mL(恢复到原状况),将此450 mL气体通过足量NaOH溶液后,溶液增重0.985 g,求原混合气体中SO2的质量。
0.961 g
(1)根据反应2SO2+O2 2SO3,在标准状况下SO3为固态,利用差量法,可假设参加反应的SO2为x mL,则有如下关系:
2SO3,在标准状况下SO3为固态,利用差量法,可假设参加反应的SO2为x mL,则有如下关系:
2SO2+O2 2SO3 减少体积(ΔV)
2SO3 减少体积(ΔV)
2 3
x (500-450)
即 ,x=
,x= mL,参加反应的SO2的物质的量为n(SO2)=
mL,参加反应的SO2的物质的量为n(SO2)= ×10-3 mol;据此生成SO3的物质的量为n(SO3)=
×10-3 mol;据此生成SO3的物质的量为n(SO3)= ×10-3 mol。
×10-3 mol。
(2)NaOH溶液吸收的气体物质为未参加反应的SO2和生成的SO3,因此未参加反应的SO2的质量为(0.985- ×10-3×80) g。
×10-3×80) g。
(3)原SO2的质量为参加反应的SO2与剩余SO2的质量之和,即m(SO2)= ×10-3×64+0.985-
×10-3×64+0.985- ×10-3×80="0.961" g。
×10-3×80="0.961" g。
 2SO3,在标准状况下SO3为固态,利用差量法,可假设参加反应的SO2为x mL,则有如下关系:
2SO3,在标准状况下SO3为固态,利用差量法,可假设参加反应的SO2为x mL,则有如下关系:2SO2+O2
 2SO3 减少体积(ΔV)
2SO3 减少体积(ΔV)2 3
x (500-450)
即
 ,x=
,x= mL,参加反应的SO2的物质的量为n(SO2)=
mL,参加反应的SO2的物质的量为n(SO2)= ×10-3 mol;据此生成SO3的物质的量为n(SO3)=
×10-3 mol;据此生成SO3的物质的量为n(SO3)= ×10-3 mol。
×10-3 mol。(2)NaOH溶液吸收的气体物质为未参加反应的SO2和生成的SO3,因此未参加反应的SO2的质量为(0.985-
 ×10-3×80) g。
×10-3×80) g。(3)原SO2的质量为参加反应的SO2与剩余SO2的质量之和,即m(SO2)=
 ×10-3×64+0.985-
×10-3×64+0.985- ×10-3×80="0.961" g。
×10-3×80="0.961" g。
练习册系列答案
相关题目