题目内容
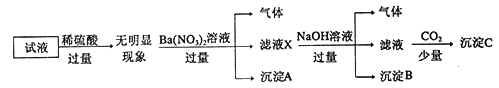
【题目】某试液中只可能含有K+、NH4+、Fe2+、A13+、Cl-、SO42-、CO32-、A1O2-中的若干种离子,离子浓度均为0.1mol/L,某同学进行了如下实验: 下列说法正确的是
A. 原溶液中存在NH4+、Fe2+、Cl-、SO42-
B. 滤液X中大量存在的阳离子有NH4+、Fe2+和Ba2+
C. 无法确定沉淀C的成分
D. 无法确定原试液中是否含有Al3+、Cl-
【答案】A
【解析】加入过量稀硫酸无明显变化,说明不含碳酸根离子,不含Ba2+,不含AlO2-;加入硝酸钡有气体生成,因为前面已经加入了硫酸,硝酸根离子在酸性条件下具有强氧化性,说明有亚铁离子存在且被氧化,沉淀为硫酸钡;加入NaOH有气体,说明存在铵根离子,生成的气体为氨气,沉淀B为红褐色氢氧化铁沉淀;通入CO2产生沉淀,说明存在Al3+,沉淀C为氢氧化铝。因为存在的离子浓度均为0.1molL-1,从电荷的角度出发,只能含有NH4+、Fe2+、Cl-、SO42-才能保证电荷守恒,K+必然不能存在。故A、原溶液中存在Al3+、NH4+、Fe2+、Cl-、SO42-,选项A正确;B、滤液X中大量存在的阳离子有NH4+、Fe2+和Al3+,选项B错误;C、沉淀C为氢氧化铝,选项C错误;D、原试液中含有Al3+、Cl-,选项D错误。答案选A。

练习册系列答案
相关题目
【题目】下表中金属的冶炼原理与方法不完全正确的是( )
选项 | 冶炼原理 | 方法 |
A | 2HgO=2Hg+O2 | 热分解法 |
B | 2Al2O3 (熔融)=4Al+3O2 | 电解法 |
C | Cu2S+O2=2Cu+SO2 | 热分解法 |
D | Fe2O3 +2Al=2Fe+Al2O3 | 热还原法 |
A. AB. BC. CD. D