题目内容
【题目】用双线桥分析下列氧化还原反应中化合价变化、得失电子情况,并指出氧化剂和还原剂是什么.
(1)H2+CuO═Cu+H2O;上面反应中,氧化剂是:还原剂是: , “双线桥”表示电子转移方向及数目为
(2)C+2CuO═2Cu+CO2↑;该反应中氧化剂是:还原剂是: . 双线桥法为: ,
【答案】
(1)CuO;H2;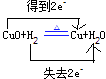
(2)CuO;C;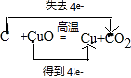
【解析】解:H2+CuO═Cu+H2O中,H元素的化合价升高,H2为还原剂,CuO为氧化极,“双线桥”表示电子转移方向及数目为 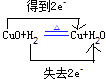 ,所以答案是:CuO;H2;
,所以答案是:CuO;H2;  ;(2)C+2CuO═2Cu+CO2↑中,氧化铜中Cu的化合价由+2价降到0价,一氧化碳中C的化合价由+2升高到+4价,一氧化碳是还原剂,氧化铜为氧化剂,双线桥法为:
;(2)C+2CuO═2Cu+CO2↑中,氧化铜中Cu的化合价由+2价降到0价,一氧化碳中C的化合价由+2升高到+4价,一氧化碳是还原剂,氧化铜为氧化剂,双线桥法为:  ,所以答案是:CuO;C;
,所以答案是:CuO;C;  .
.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目