题目内容
能源问题是当前世界各国所面临的严重问题,同时全球气候变暖,生态环境问题日益突出,开发氢能、研制燃料电池、发展低碳经济是化学工作者的研究方向.I.氢气通常用生产水煤气方法制得.其中CO(g)+H2O(g)?CO2(g)+H2(g)△H<0.在850℃时,平衡常数K=1.
(1)若降低温度到750℃时,达到平衡时K______1(填“大于”、“小于”或“等于”)
(2)850℃时,若向一容积可变的密闭容器中同时充入1.0mol CO、3mol H2O、1.0mol CO2和x mol H2,则:
①当x=5.0时,上述反应向______(填“正反应”或“逆反应”)方向进行.
②若要使上述反应开始时向正反应方向进行,则x应满足的条件是______.
③在850℃时,若设x=5.0和x=6.0,其它物质的投料不变,当上述反应达到平衡后,测得H2的体积分数分别为a%、b%,则a______b(填“大于”、“小于”或“等于”)
II.已知4.6g液态乙醇完全燃烧生成二氧化碳和液态水放出热量136kJ,1mol液态水转化为气体水吸收44kJ的热量.
(3)请写出乙醇燃烧生成气态水的热化学方程式______.
(4)将0.1mol乙醇在足量氧气中燃烧,得到的气体全部通入到100mL 3mol/L NaOH溶液中,忽略HCO-3的电离,则所得溶液中c(CO2-3)______c(HCO-3)(填“大于”、“小于”或“等于”,)原因是______(用文字叙述).
【答案】分析:I.(1)降低温度,平衡向放热方向移动,该反应为放热反应,即向正反应方向移动;
(2)反应在同一容器内进行,体积相同,方程式中各物质的化学计量数都是1,所以在以下计算中均可用物质的量数值代替浓度数值.
①求出此时的浓度商Qc,与平衡常数相比,判断平衡移动方向;
②用x表示出浓度商Qc,平衡向正反应方向移动,浓度商小于平衡常数;
③增大一种生产物(氢气)的体积分数,平衡向逆反应方向移动,平衡移动的结果是降低这种增大的幅度,故平衡后氢气的体积分数还是大于原来的;
II.(3)先求出1mol液态乙醇完全燃烧生成二氧化碳和气态水放出热量,再根据书写热化学方程式的方法书写;
(4)计算出反应生成的碳酸钠与碳酸氢钠的物质的量,再根据 CO32-与HCO3-水解程度判断.
解答:解:I.(1)降低温度,平衡向放热方向移动,该反应为放热反应,即向正反应方向移动,平衡常数K增大,故答案为:大于;
(2)①此时的浓度商Qc=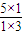 =1.67,大于平衡常数1,故平衡向逆反应方向移动,故答案为:逆反应;
=1.67,大于平衡常数1,故平衡向逆反应方向移动,故答案为:逆反应;
②平衡向正反应方向移动,浓度商小于平衡常数,即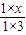 <1,解得x<3,故答案为:x<3;
<1,解得x<3,故答案为:x<3;
③增大一种生产物(氢气)的体积分数,平衡向逆反应方向移动,平衡移动的结果是降低这种增大的幅度,故平衡后氢气的体积分数还是大于原来的,故答案为:小于;
II.(3)4.6g乙醇的物质的量为 =0.1mol,
=0.1mol,
所以1mol液态乙醇完全燃烧生成二氧化碳和液态水放出热量为136kJ?mol×0.1mol×10=1360kJ,
1mol液态乙醇完全燃烧生成3mol水,3mol液态水转化为气体水吸收热量44kJ×3=132kJ,
所以1mol液态乙醇完全燃烧生成二氧化碳和气态水放出热量为1360kJ-132kJ=1228kJ,
所以乙醇燃烧生成气态水的热化学方程式为C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g)△H=-1228kJ/mol,
故答案为:C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g)△H=-1228kJ/mol;
(4)令碳酸钠的物质的量为xmol,碳酸氢钠的物质的量为ymol,则:
根据碳原子守恒有xmol+ymol=0.2mol,
根据钠原子守恒有2xmol+ymol=0.1L×3mol/L,
联立方程,解得x=0.1,y=0.1,
生成的碳酸钠与碳酸氢钠的物质的量相等,CO32-水解程度大于HCO3-水解程度,故溶液中c(CO2-3)小于c(HCO-3).
故答案为:小于;生成的碳酸钠与碳酸氢钠的物质的量相等,CO32-水解程度大于HCO3-水解程度.
点评:注意化学平衡常数只与温度有关,与反应物浓度、是否使用催化剂无关,温度不变,化学平衡常数不变.
(2)反应在同一容器内进行,体积相同,方程式中各物质的化学计量数都是1,所以在以下计算中均可用物质的量数值代替浓度数值.
①求出此时的浓度商Qc,与平衡常数相比,判断平衡移动方向;
②用x表示出浓度商Qc,平衡向正反应方向移动,浓度商小于平衡常数;
③增大一种生产物(氢气)的体积分数,平衡向逆反应方向移动,平衡移动的结果是降低这种增大的幅度,故平衡后氢气的体积分数还是大于原来的;
II.(3)先求出1mol液态乙醇完全燃烧生成二氧化碳和气态水放出热量,再根据书写热化学方程式的方法书写;
(4)计算出反应生成的碳酸钠与碳酸氢钠的物质的量,再根据 CO32-与HCO3-水解程度判断.
解答:解:I.(1)降低温度,平衡向放热方向移动,该反应为放热反应,即向正反应方向移动,平衡常数K增大,故答案为:大于;
(2)①此时的浓度商Qc=
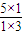 =1.67,大于平衡常数1,故平衡向逆反应方向移动,故答案为:逆反应;
=1.67,大于平衡常数1,故平衡向逆反应方向移动,故答案为:逆反应;②平衡向正反应方向移动,浓度商小于平衡常数,即
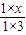 <1,解得x<3,故答案为:x<3;
<1,解得x<3,故答案为:x<3;③增大一种生产物(氢气)的体积分数,平衡向逆反应方向移动,平衡移动的结果是降低这种增大的幅度,故平衡后氢气的体积分数还是大于原来的,故答案为:小于;
II.(3)4.6g乙醇的物质的量为
 =0.1mol,
=0.1mol,所以1mol液态乙醇完全燃烧生成二氧化碳和液态水放出热量为136kJ?mol×0.1mol×10=1360kJ,
1mol液态乙醇完全燃烧生成3mol水,3mol液态水转化为气体水吸收热量44kJ×3=132kJ,
所以1mol液态乙醇完全燃烧生成二氧化碳和气态水放出热量为1360kJ-132kJ=1228kJ,
所以乙醇燃烧生成气态水的热化学方程式为C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g)△H=-1228kJ/mol,
故答案为:C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g)△H=-1228kJ/mol;
(4)令碳酸钠的物质的量为xmol,碳酸氢钠的物质的量为ymol,则:
根据碳原子守恒有xmol+ymol=0.2mol,
根据钠原子守恒有2xmol+ymol=0.1L×3mol/L,
联立方程,解得x=0.1,y=0.1,
生成的碳酸钠与碳酸氢钠的物质的量相等,CO32-水解程度大于HCO3-水解程度,故溶液中c(CO2-3)小于c(HCO-3).
故答案为:小于;生成的碳酸钠与碳酸氢钠的物质的量相等,CO32-水解程度大于HCO3-水解程度.
点评:注意化学平衡常数只与温度有关,与反应物浓度、是否使用催化剂无关,温度不变,化学平衡常数不变.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 CO2(g)+H2(g)
CO2(g)+H2(g) 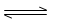 CO2(g)+H2(g)
CO2(g)+H2(g)