题目内容
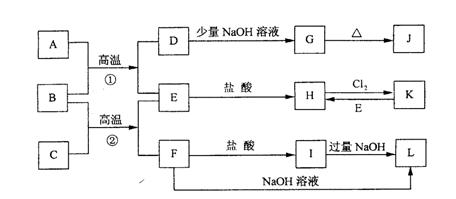
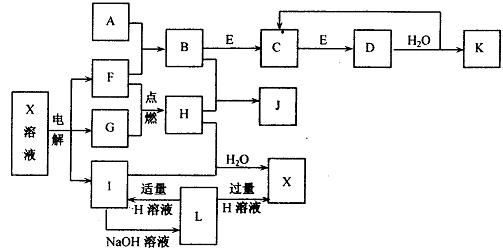
下表所示为部分短周期元素的原子半径及主要化合价,根据表中信息判断以下叙述正确的是
A.A、B的单质与稀盐酸反应速率B>A
B.D、E形成的简单离子的还原性E->D-
C.气态氢化物的稳定性HD<H2C
D.最高价氧化物对应的水化物的酸性 H2CO4>HEO4
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.071 | 0.099 |
| 主要化合价 | +2 | +3 | +6、-2 | -1 | -1 |
B.D、E形成的简单离子的还原性E->D-
C.气态氢化物的稳定性HD<H2C
D.最高价氧化物对应的水化物的酸性 H2CO4>HEO4
B
试题分析:根据元素的主要化合价和原子半径可知,A是Mg,B是Al,C是S,D是F,E是Cl。A不正确,反应速率快的是Mg;非金属性越强,相应阴离子的还原性越弱,非金属性是F大于Cl,B正确;非金属性越强,氢化物的稳定性越强,Cl的非金属性强于S的,所以氯化氢的稳定性强于H2S的,C不正确;非金属性越强,最高价氧化物的水化物的酸性越强,所以D不正确,应该是高氯酸强于硫酸的,答案选B。
点评:该题以“周期表中元素的推断”为载体,考查学生对元素周期表的熟悉程度及其对表中各元素性质和相应原子结构的周期性递变规律的认识和掌握程度。考查了学生对物质结构与性质关系以及运用元素周期律解决具体化学问题的能力。

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目