题目内容
天然气、煤炭气(CO、H2)的研究在世界上相当普遍。其中天然气和二氧化碳可合成二甲醚,二甲醚与水蒸气制氢气作为燃料电池的氢能源,比其他制氢技术更有优势。主要反应为:
①CH3OCH3(g)
+H2O(g) 2CH3OH(g) △H=
37Kj·mol-1
2CH3OH(g) △H=
37Kj·mol-1
②CH3OH(g)+H2O(g)
 3 H2(g)+CO2(g) △H =49Kj·mol-1
3 H2(g)+CO2(g) △H =49Kj·mol-1
③CO2(g)
+H2(g)  CO(g)
+H2O(g) △H=41.3Kj·mol-1
CO(g)
+H2O(g) △H=41.3Kj·mol-1
其中反应③是主要的副反应,产生的CO对燃料电池Pt电极有不利影响。
请回答下列问题:
(1)二甲醚可以通过天然气和CO2合成制得,该反应的化学方程式为 。
(2)CH3OCH3(g)与水蒸气制氢气的热化学方程式为 。
(3)下列采取的措施和解释正确的是 。(填字母序号)
A.反应过程在低温进行,可减少CO的产生
B.增加进水量,有利于二甲醚的转化,并减少CO的产生
C.选择在高温具有较高活性的催化剂,有助于提高反应②CH3OH的转化率
D.体系压强升高,虽然对制取氢气不利,但能减少CO的产生
(4)煤炭气在一定条件下可合成燃料电池的另一种重要原料甲醇,反应的化学方程式为:
CO (g) +2H2(g)  CH3OH(g)
△H <0。现将l0mol CO与20mol H2置于密闭容器中,在催化剂作用下发生反应生成甲醇,CO的平衡转化率(
CH3OH(g)
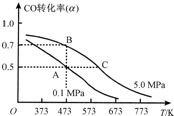
△H <0。现将l0mol CO与20mol H2置于密闭容器中,在催化剂作用下发生反应生成甲醇,CO的平衡转化率( )与温度、压强的关系如下图所示。
)与温度、压强的关系如下图所示。

①自反应开始到达平衡状态所需的时间tA tB(填“大于”、“小于”或“等于”)。
②A、C两点的平衡常数KA KC(填“大于”、“小于”或“等于”)。
(5)某工作温度为650oC的熔融盐燃料电池,是以镍合金为电极材料,负极通人煤炭气(CO、H2),正极通人空气与CO2的混合气体,用一定比例的Li2CO3和Na2CO3混合物做电解质。请写出正极的电极反应式 ____ 。
(1)3CH4+CO2→2CH3OCH3
(2)
CH3OCH3(g)
+3H2O(g)  6H2(g)+2CO2(g) △H= 135kJ·mol-1
6H2(g)+2CO2(g) △H= 135kJ·mol-1
(3) ABD (4)①大于 ②大于 (5)O2+4e-+2CO2= 2CO32-
【解析】
试题分析:本题是有关化学反应原理的综合题。(1)根据原子守恒书写方程式;(2)给出的三个方程式中第③是副反应,所以CH3OCH3(g)与水蒸气制氢气的热化学方程式应是①+2②得到,△H也这样计算。
CH3OCH3(g) +3H2O(g) 6H2(g)+2CO2(g)
△H= 135kJ·mol-1
6H2(g)+2CO2(g)
△H= 135kJ·mol-1
(3)A、反应③是吸热反应,降低温度平衡逆向移动,减少CO的产生,正确;B、对反应①、②来说,水是反应物,增加进水量,促进二甲醚的转化;对于反应③,水是生成物,增加水的量会抑制该反应正向进行,减少CO的产生,正确;C、催化剂不能改变反应物的转化率,只能改变反应速率,错误;D、增大压强对于反应②逆向移动,制取的氢气量减少,但对于反应③,增大压强水的浓度增大,使平衡逆向移动,减少CO的产生,正确。(4)B点压强大,反应速率快,先达到平衡,用时少;K只和温度有关,温度高,该反应逆向移动,K值大,所以KA 大于KC;书写电极反应式时要确定正极反应物和产物,要明确介质,确定氧的存在微粒。
考点:考查化学反应原理中的热化学书写、平衡移动、电极反应式书写等方面的内容。

 (2013?无锡一模)天然气、煤炭气(CO、H2)的研究在世界上相当普遍.其中天然气和二氧化碳可合成二甲醚,二甲醚与水蒸气制氢气作为燃料电池的氢能源,比其他制氢技术更有优势.主要反应为:
(2013?无锡一模)天然气、煤炭气(CO、H2)的研究在世界上相当普遍.其中天然气和二氧化碳可合成二甲醚,二甲醚与水蒸气制氢气作为燃料电池的氢能源,比其他制氢技术更有优势.主要反应为: