题目内容
关于如图所示的原电池,下列说法错误的是
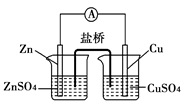

| A.电子从锌电极通过电流计流向铜电极 |
| B.盐桥中的阳离子向硫酸铜溶液中迁移 |
| C.锌电极发生氧化反应,铜电极发生还原反应 |
| D.铜电极上发生的电极反应为2H++2e-===H2↑ |
D
试题分析:该原电池为铜锌原电池,锌为负极,发生了氧化反应,电极反应为Zn-2e-===Zn2+,铜电极为正极,发生了还原反应,电极反应为Cu2++2e-=Cu。A正确,电子从锌电极通过电流计流向铜电极,电流为从铜极通过导线流向锌极;B正确,因为铜极消耗了大量的阳离子,所以盐桥中的阳离子向硫酸铜溶液中迁移;C正确,锌电极发生氧化反应,铜电极发生还原反应,D则错误,铜电极上发生的电极反应为Cu2++2e-=Cu。本题的答案选择D。
点评:本题考查了原电池,原电池是高考考查的重点和难点,本题难度适中。

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
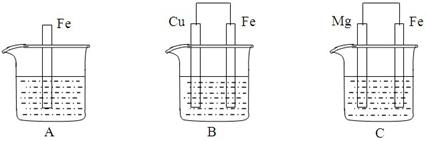
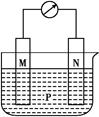

 2Ni(OH) 2根据此反应式判断,此电池放电时,负极上发生反应的物质是 ( )
2Ni(OH) 2根据此反应式判断,此电池放电时,负极上发生反应的物质是 ( )