题目内容
【题目】标准状况下将![]() 气体缓缓地通入到含2molKOH、
气体缓缓地通入到含2molKOH、![]() 和
和![]() 的混合溶液中直至过量,生成沉淀的物质的量与所通
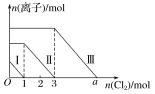
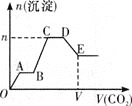
的混合溶液中直至过量,生成沉淀的物质的量与所通![]() 的体积关系如图所示。下列关于整个反应进程中的各种描述正确的是
的体积关系如图所示。下列关于整个反应进程中的各种描述正确的是
A.![]() 段和
段和![]() 段发生的反应相同
段发生的反应相同
B.![]() 段发生反应的离子方程式为:
段发生反应的离子方程式为:![]()
C.![]() ,
,![]()
D.D点所得溶液中离子浓度的关系为:![]()
【答案】C
【解析】
通入![]() 后立刻发生反应
后立刻发生反应![]() 生成沉淀
生成沉淀![]() ,将
,将![]() 消耗完毕,然后发生反应
消耗完毕,然后发生反应![]() ,故此段沉淀的量保持不变,然后又发生反应:
,故此段沉淀的量保持不变,然后又发生反应:![]() ,沉淀量达最大后,再发生反应:
,沉淀量达最大后,再发生反应:![]() ,最后发生反应
,最后发生反应![]() ,沉淀部分溶解,直至沉淀质量不变,由此答题。
,沉淀部分溶解,直至沉淀质量不变,由此答题。
A、根据上述分析可知,![]() 段发生
段发生![]() ,离子方程式
,离子方程式![]() ,
,![]() 段发生反应为:
段发生反应为:![]() ,两阶段反应不相同,故A错误;
,两阶段反应不相同,故A错误;
B、由上述分析可知,![]() 段反应的离子方程式为:
段反应的离子方程式为:![]() ,故B错误;
,故B错误;
C、结合上述分析可知,到V处时溶液中的溶质是碳酸氢钾、碳酸氢钡,由原子守恒可知,![]() ,标准况下
,标准况下![]() 的体积为
的体积为![]() ,C点时的沉淀为碳酸钡和氢氧化铝,故n值就是Ba、Al两原子的物质的量之和3mol,故C正确;
,C点时的沉淀为碳酸钡和氢氧化铝,故n值就是Ba、Al两原子的物质的量之和3mol,故C正确;
D、D点溶液中的溶质是碳酸氢钾,所得溶液中离子浓度的关系:![]() ,故D错误;
,故D错误;
故答案为:C。

练习册系列答案
 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
一课一练课时达标系列答案
相关题目