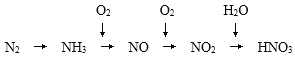题目内容
【题目】以有机物A合成聚酯类高分子化合物F的路线如下图所示:

已知:①RCH=CH2 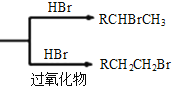 ②丙酮能被KMnO4(H+)氧化,使之褪色
②丙酮能被KMnO4(H+)氧化,使之褪色
(1)A生成B的反应类型为_______,C中含氧官能团的名称为_______。
(2)G是与CH3OH相对分子质量相差56的同系物,且不能使KMnO4(H+)褪色,G的名称为__________________
(3)检验A分子碳碳双键的方法_______________________________________________。
(4)D与NaOH水溶液反应的化学方程式为_____________________________________。
(5)E在一定条件下还可以合成含有六元环结构的H,则H的结构简式为____________。
(6)若F的平均相对分子质量为25200,则其平均聚合度为_______________
(7)满足下列条件的C的同分异构体有____________种(不考虑立体异构)。
①含有1个六元碳环,且环上相邻4个碳原子上各连有一个取代基
②1mol该物质与新制氢氧化铜悬浊液反应产生2mol砖红色沉淀
(8)写出以![]() 为原料(其他试剂任选)制备化合物
为原料(其他试剂任选)制备化合物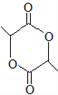 的合成路线,请用以下方式表示:
的合成路线,请用以下方式表示:![]() 目标产物。__________________
目标产物。__________________
【答案】 氧化反应 酯基 2-甲基-2-丁醇 取少量A,加入足量新制Cu(OH)2悬浊液,加热充分反应;取实验后试管中的清液少许,向其中加入稀硫酸酸化,再加入KMnO4溶液(或溴水),KMnO4溶液(或溴水)褪色,说明A中含碳碳双键 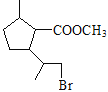 +2NaOH
+2NaOH![]()
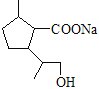 +CH3OH+NaBr
+CH3OH+NaBr 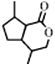 150 12种
150 12种 ![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
【解析】分析:根据B→C的试剂和条件以及C的结构简式,可逆推出B的结构简式为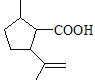 ;根据题给已知①,C与HBr在过氧化物作用下发生加成反应生成的D的结构简式为
;根据题给已知①,C与HBr在过氧化物作用下发生加成反应生成的D的结构简式为 ;D与NaOH水溶液、加热发生水解反应,产物酸化后生成的E的结构简式为
;D与NaOH水溶液、加热发生水解反应,产物酸化后生成的E的结构简式为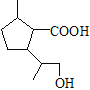 ;E中含羧基和羟基,E发生缩聚反应生成聚酯类高分子化合物F,F的结构简式为
;E中含羧基和羟基,E发生缩聚反应生成聚酯类高分子化合物F,F的结构简式为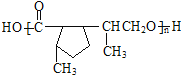 。
。
详解:根据B→C的试剂和条件以及C的结构简式,可逆推出B的结构简式为 ;根据题给已知①,C与HBr在过氧化物作用下发生加成反应生成的D的结构简式为
;根据题给已知①,C与HBr在过氧化物作用下发生加成反应生成的D的结构简式为 ;D与NaOH水溶液、加热发生水解反应,产物酸化后生成的E的结构简式为
;D与NaOH水溶液、加热发生水解反应,产物酸化后生成的E的结构简式为 ;E中含羧基和羟基,E发生缩聚反应生成聚酯类高分子化合物F,F的结构简式为
;E中含羧基和羟基,E发生缩聚反应生成聚酯类高分子化合物F,F的结构简式为 。
。
(1)对比A、B的结构简式,A→B是A中醛基氧化成B中羧基,A生成B的反应类型为氧化反应。根据C的结构简式,C中含氧官能团的名称为酯基。
(2)与CH3OH相对分子质量相差56的同系物为C5H11OH,G不能使KMnO4(H+)褪色,根据已知②“丙酮能被KMnO4(H+)氧化,使之褪色”以及醛类能使KMnO4(H+)褪色,G的结构简式为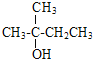 ,根据醇的系统命名原则,G的名称为2-甲基-2-丁醇。
,根据醇的系统命名原则,G的名称为2-甲基-2-丁醇。
(3)检验A中的碳碳双键可用溴水或酸性KMnO4溶液,由于A中的醛基也能使溴水或酸性KMnO4溶液褪色而干扰碳碳双键的检验,所以先用新制Cu(OH)2悬浊液或银氨溶液与醛基反应排除醛基的干扰。检验A分子碳碳双键的方法:取少量A,加入足量新制Cu(OH)2悬浊液,加热充分反应;取实验后试管中的清液少许,向其中加入稀硫酸酸化,再加入KMnO4溶液(或溴水),KMnO4溶液(或溴水)褪色,说明A中含碳碳双键。
(4)D的结构简式为 ,D与NaOH水溶液反应的化学方程式为
,D与NaOH水溶液反应的化学方程式为 +2NaOH
+2NaOH![]()
 +CH3OH+NaBr。
+CH3OH+NaBr。
(5)E的结构简式为 ,E中含羧基和羟基,E发生分子内酯化生成含有六元环结构的H,H的结构简式为
,E中含羧基和羟基,E发生分子内酯化生成含有六元环结构的H,H的结构简式为 。
。
(6)F的结构简式为 ,F的链节的式量为168,F的平均相对分子质量为25200,F的平均聚合度为
,F的链节的式量为168,F的平均相对分子质量为25200,F的平均聚合度为![]() =150。
=150。
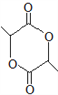
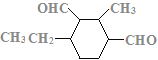
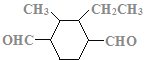
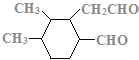
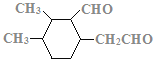
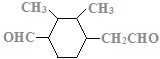
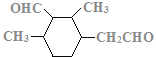
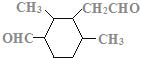
(7)C的结构简式为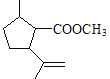 ,C的不饱和度为3,C的分子式为C11H18O2,1molC的同分异构体与新制Cu(OH)2悬浊液反应产生2mol砖红色沉淀,C的同分异构体中含2个醛基;C的同分异构体中含1个六元碳环,且环上相邻4个碳原子上各连有一个取代基;符合①②两个条件的C的同分异构体有:
,C的不饱和度为3,C的分子式为C11H18O2,1molC的同分异构体与新制Cu(OH)2悬浊液反应产生2mol砖红色沉淀,C的同分异构体中含2个醛基;C的同分异构体中含1个六元碳环,且环上相邻4个碳原子上各连有一个取代基;符合①②两个条件的C的同分异构体有: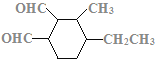 、
、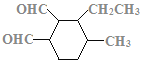 、
、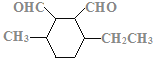 、
、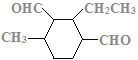 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、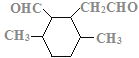 ,共12种。
,共12种。
(8) 中官能团为酯基,
中官能团为酯基, 由
由![]() 通过酯化反应生成;
通过酯化反应生成;![]() 与原料
与原料![]() 对比,碳干骨架不变,原料中醛基氧化成羧基、碳碳双键最终变为羟基,模仿A→B将
对比,碳干骨架不变,原料中醛基氧化成羧基、碳碳双键最终变为羟基,模仿A→B将![]() 氧化成
氧化成![]() ;根据已知①,
;根据已知①,![]() 与HBr发生加成反应生成
与HBr发生加成反应生成![]() ,
,![]() 水解后酸化生成
水解后酸化生成![]() ;合成路线为:
;合成路线为:![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
 。
。

 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案【题目】下列实验中,对应的现象及结论或解释均正确的是
选项 | 实验操作 | 现象 | 结论或解释 |
A | 向氢氧化铁胶体中滴加硫酸钠溶液 | 有红褐色沉淀 | 胶体遇强电解质聚沉 |
B | 将SO2通入紫色石蕊溶液中 | 溶液先变红后褪色 | SO2具有漂白性 |
C | 将灼烧至红热的铜丝插入乙醇中 | 铜丝由黑变红 | 乙醇被还原 |
D | 向氯化铝溶液中持续通入氨气 | 产生白色沉淀后溶解 | Al(OH)3与碱反应 |
A. A B. B C. C D. D