题目内容
下列有关化学用语或名称表达正确的是
A.亚硫酸的电离方程式:H2SO3 2H++SO32- 2H++SO32- |
B.乙炔的分子结构模型示意图: |
C.H2O2的电子式: |
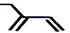
D. 的名称3-甲基-1-丁醇 的名称3-甲基-1-丁醇 |
D
解析试题分析:A、多元弱酸分步电离,错误;B、乙炔为直线型结构,错误;C、双氧水为共价化合物,不能形成离子,错误;D、正确。
考点:考查化学用语有关问题。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
科学家发现C60后,近年又合成了许多球形分子(富勒烯),如C50、C70、C120、C540等,它们互称为
| A.同种物质 | B.同分异构体 | C.同素异形体 | D.同位素 |
下列关于同温同压下的两种气体12C18O和14N2的判断正确的是
| A.体积相等时密度相等 |
| B.原子数相等时具有的中子数相等 |
| C.体积相等时具有的电子数相等 |
| D.质量相等时具有的质子数相等 |
NA代表阿伏伽德罗常数。已知C2H4和C3H6的混合物的质量为ag,则该混合物
| A.所含共用电子对数目为(a/7+1)NA |
| B.所含碳氢键数目为aNA/7 |
| C.燃烧时消耗的O2一定是33.6a/14L |
| D.所含原子总数为aNA/14 |
一定温度下,硫酸铜受热分解生成CuO、SO2、SO3和O2。已知:SO2、SO3都能被碱石灰和氢氧化钠溶液吸收。用下图装置加热硫酸铜粉末直至完全分解。若硫酸铜粉末质量为10.0 g,完全分解后,各装置的质量变化关系如下表所示。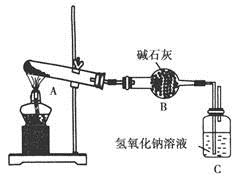
| 装置 | A(试管+粉末) | B | C |
| 反应前 | 42.0 g | 75.0 g | 140.0 g |
| 反应后 | 37.0 g | 79.5 g | 140.0 g |
请通过计算,推断出该实验条件下硫酸铜分解的化学方程式是
A.4CuSO4
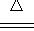 4CuO+2SO3↑+2SO2↑+O2↑
4CuO+2SO3↑+2SO2↑+O2↑B.3CuSO4
 3CuO+SO3↑+2SO2↑+O2↑
3CuO+SO3↑+2SO2↑+O2↑C.5CuSO4
 5CuO+SO3↑+4SO2↑+2O2↑
5CuO+SO3↑+4SO2↑+2O2↑D.6CuSO4
 6CuO+4SO3↑+2SO2↑+O2↑
6CuO+4SO3↑+2SO2↑+O2↑ 设NA表示阿伏加德罗常数的数值,下列有关说法中正确的是( )。
| A.15 g CH3+含电子数为10 NA |
| B.78 g Na2O2发生氧化还原反应,转移电子数一定是NA |
| C.一定条件下,向密闭容器中充入1 mol N2与3 mol H2,发生化学反应转移电子数为6 NA |
| D.22.4 L(标况下)氯气与足量的铁、铜在一定条件下发生反应,转移电子数均为2 NA |