题目内容
11.用NA表示阿伏加德罗常数的值.下列叙述中不正确的是( )| A. | 分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA | |
| B. | 在常温常压下,1 mol 氦气含有的原子数为NA | |
| C. | 常温常压下,22.4L氯气与足量金属钠充分反应,转移的电子数为2NA | |
| D. | 常温常压下,46g的NO2和N2O4混合气体含有的原子数为3NA |
分析 A、二氧化氮和二氧化碳中均含2个氧原子;
B、氦气为单原子分子;
C、常温常压下,气体摩尔体积大于22.4L/mol;
D、NO2和N2O4的最简式均为NO2.
解答 解:A、二氧化氮和二氧化碳中均含2个氧原子,故NA个NO2和CO2混合气体中含2NA个氧原子,与两者的比例无关,故A正确;
B、氦气为单原子分子,故1mol氦气中含1mol氦原子即NA个,故B正确;
C、常温常压下,气体摩尔体积大于22.4L/mol,故22.4L氯气的物质的量小于1mol,则与金属钠反应后转移的电子小于2NA个,故C错误;
D、NO2和N2O4的最简式均为NO2,故46g混合物中含有的NO2的物质的量为n=$\frac{46g}{46g/mol}$=1mol,则含3mol原子即3NA个,故D正确.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 快捷英语周周练系列答案
快捷英语周周练系列答案
相关题目
1.在1.0L密闭容器中放入1.0molX(g),在一定温度进行如下反应:X(g)?Y(g)+Z(g)△H=akJ.mol-1反应时间(t)与容器内气体总压强(p)的数据见下表:
回答下列问题:
(1)实验测得,随温度的升高反应的平衡常数K增大,则△H>0(填>、<或=)
(2)其他条件不变时,为使平衡向右移动,采用的下列措施可行的是BD.
A.缩小容器容积 B.及时分离出Y、Z C.使用合理的催化剂 D.升高体系温度
(3)计算平衡时X的转化率为50%,该温度下反应的平衡常数值为:0.5.
(4)由总压强p和起始压强po表示反应体系的总物质的量n(总)和反应物X的物质的量n(X),则n(总)=$\frac{p}{{p}_{0}}$mol,n(X)=(2-$\frac{p}{{p}_{0}}$)mol,反应物X的转化率a(X)的表达式为($\frac{p}{{p}_{0}}$-1)×100%.
| 时间t/h | 0 | 1 | 2 | 4 | 8 | 16 |
| 总压强p/100kPa | 4.00 | 4.20 | 4.50 | 5.20 | 6.00 | 6.00 |
(1)实验测得,随温度的升高反应的平衡常数K增大,则△H>0(填>、<或=)
(2)其他条件不变时,为使平衡向右移动,采用的下列措施可行的是BD.
A.缩小容器容积 B.及时分离出Y、Z C.使用合理的催化剂 D.升高体系温度
(3)计算平衡时X的转化率为50%,该温度下反应的平衡常数值为:0.5.
(4)由总压强p和起始压强po表示反应体系的总物质的量n(总)和反应物X的物质的量n(X),则n(总)=$\frac{p}{{p}_{0}}$mol,n(X)=(2-$\frac{p}{{p}_{0}}$)mol,反应物X的转化率a(X)的表达式为($\frac{p}{{p}_{0}}$-1)×100%.
19.在进行中和反应的反应热测定的实验中不需要用到的仪器是( )
| A. | 天平 | B. | 温度计 | C. | 环形玻璃搅拌棒 | D. | 量筒 |
6.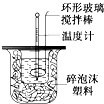 利用如图装置测定中和热的实验步骤如下:
利用如图装置测定中和热的实验步骤如下:
①用量筒量取50mL 0.25mol/L硫酸倒入小烧杯中,测出硫酸温度;
②用另一量筒量取50mL 0.55mol/L NaOH溶液,并用另一温度计测出其温度;
③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测出混合液最高温度. 回答下列问题:
(1)写出稀硫酸和稀氢氧化钠溶液反应表示中和热的热化学方程式(中和热数值为57.3kJ/mol):$\frac{1}{2}$H2SO4(aq)+NaOH(aq)═$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-57.3kJ•mol-1.
(2)倒入NaOH溶液的正确操作是:C. (从下列选项中选出).
A.沿玻璃棒缓慢倒入 B.分三次少量倒入C.一次迅速倒入
(3)实验数据如下表:
①请填写下表中的空白:
②近似认为0.55mol/L NaOH溶液和0.25mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g•℃).则中和热△H=-56.8kJ/mol ( 取小数点后一位).
③上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是(填字母)a、b、c.
a.实验装置保温、隔热效果差
b.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中.
 利用如图装置测定中和热的实验步骤如下:
利用如图装置测定中和热的实验步骤如下:①用量筒量取50mL 0.25mol/L硫酸倒入小烧杯中,测出硫酸温度;
②用另一量筒量取50mL 0.55mol/L NaOH溶液,并用另一温度计测出其温度;
③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测出混合液最高温度. 回答下列问题:
(1)写出稀硫酸和稀氢氧化钠溶液反应表示中和热的热化学方程式(中和热数值为57.3kJ/mol):$\frac{1}{2}$H2SO4(aq)+NaOH(aq)═$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-57.3kJ•mol-1.
(2)倒入NaOH溶液的正确操作是:C. (从下列选项中选出).
A.沿玻璃棒缓慢倒入 B.分三次少量倒入C.一次迅速倒入
(3)实验数据如下表:
①请填写下表中的空白:
| 温度 实验 次数 | 起始温度t1℃ | 终止温度t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 29.5 | |
| 2 | 27.0 | 27.4 | 27.2 | 32.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.2 | |
| 4 | 26.4 | 26.2 | 26.3 | 29.8 | |
③上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是(填字母)a、b、c.
a.实验装置保温、隔热效果差
b.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中.
16.下列叙述中正确的是( )
| A. | 能电离出H+的化合物都是酸 | |
| B. | 胶体区别于其他分散系的本质特征是能产生丁达尔效应 | |
| C. | 冰水混合物是电解质 | |
| D. | 强电解质溶液的导电能力一定强 |
1.对于平衡CO2(g)═CO2(aq)△H<0,为增大CO2在水中的溶解度,应采用的方法是( )
| A. | 增加压强 | B. | 升高温度 | C. | 不断搅拌 | D. | 升温减压 |
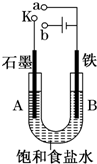 某课外活动小组用如图装置进行实验,试回答下列问题.
某课外活动小组用如图装置进行实验,试回答下列问题.