题目内容
【题目】如图所示,甲池的总反应式为:CH4+2O2+2KOU=K2CO3+3H2O,下列说法正确的是( )
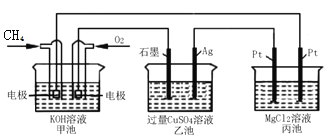
A. 甲池是电能转化为化学能的装置,乙、丙池是化学能转化电能的装置
B. 甲池中正极的电极反应式是O2+4e-+4H+=2H2O
C. 反应过程中,乙池的pH逐渐减小
D. 甲池中消耗O2的体积与丙池生成气体的总体积在相同条件下的比值为1∶2
【答案】C
【解析】
A、甲池是燃料电池,是化学能转化为电能的装置,乙、丙池是电解池,是将电能转化为化学能的装置,A错误;B、在燃料电池中,负极是甲醇发生失电子的氧化反应,正极是氧气得到电子的还原反应,在碱性电解质下的电极反应为O2+2H2O+4e-=4OH-,B错误;C、电解池乙池中,电解后生成硫酸、铜和氧气,pH逐渐减小,C正确;D、甲池中根据电极反应:O2+2H2O+4e-=4OH-,所以如果消耗1mol氧气,则转移电子4mol,根据丙装置可知生成的气体是氢气和氯气,因此根据电子守恒可知甲池中消耗O2的体积与丙池生成气体的总体积在相同条件下的比值为1∶1,D错误,答案选C。

练习册系列答案
 快捷英语周周练系列答案
快捷英语周周练系列答案
相关题目