题目内容
18. 纯净物 X、Y、Z 转化关系如右图所示,下列判断不正确的是( )
纯净物 X、Y、Z 转化关系如右图所示,下列判断不正确的是( )| A. | X 可能是金属铜 | B. | Y 可能是氢气 | ||
| C. | Z 不可能是氯化钠 | D. | Z 可能是三氧化硫 |
分析 A.电解氯化铜溶液可以得到Cu与氯气,二者反应生成氯化铜;
B.电解HCl溶液生成氢气与氯气,二者反应又得到HCl;
C.电解氯化钠溶液得到氢氧化钠、氢气与氯气;
D.三氧化硫溶于水得到硫酸,电解硫酸溶液得到氢气与氧气.
解答 解:A.电解氯化铜溶液可以得到Cu与氯气,二者反应生成氯化铜,则X可以为Cu,故A正确;
B.电解HCl溶液生成氢气与氯气,二者反应又得到HCl,Y可以为氢气,故B正确;
C.电解氯化钠溶液得到氢氧化钠、氢气与氯气,与图中转化关系不符合,故Z不能为氯化钠溶液,故C正确;
D.三氧化硫溶于水得到硫酸,电解硫酸溶液得到氢气与氧气,与图中转化关系不符合,故D错误,
故选:D.
点评 本题考查无机物推断,属于验证型题目,需要学生熟练掌握元素化合物知识与电解原理,难度中等.

练习册系列答案
相关题目
8.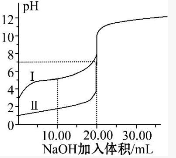 室温下,用0.100mol•L-1NaOH溶液分别滴定20.00mL 0.100mol•L-1的盐酸和醋酸,滴定曲线如图所示.下列说法正确的是( )
室温下,用0.100mol•L-1NaOH溶液分别滴定20.00mL 0.100mol•L-1的盐酸和醋酸,滴定曲线如图所示.下列说法正确的是( )
 室温下,用0.100mol•L-1NaOH溶液分别滴定20.00mL 0.100mol•L-1的盐酸和醋酸,滴定曲线如图所示.下列说法正确的是( )
室温下,用0.100mol•L-1NaOH溶液分别滴定20.00mL 0.100mol•L-1的盐酸和醋酸,滴定曲线如图所示.下列说法正确的是( )| A. | Ⅰ、Ⅱ分别表示盐酸和醋酸的滴定曲线 | |
| B. | V(NaOH)=10.00 mL时,QUOTE>1 | |
| C. | 当V(NaOH)=20.00 mL时,两种酸溶液的pH均等于7 | |
| D. | V(NaOH)=20.00 mL时,c(Cl-)<c(CH3COO-) |
9.经氯气消毒的自来水,用以配制以下溶液,不会使溶液变质的是( )
| A. | AgNO3溶液 | B. | FeCl2溶液 | C. | Na2CO3溶液 | D. | NaCl溶液 |
6.有Fe2+、NO${\;}_{3}^{-}$、Fe3+、NH${\;}_{4}^{+}$、H+和H2O六种粒子,属于同一氧化还原反应中的反应物和生成物,下列叙述不正确的是( )
| A. | 氧化剂和还原剂的物质的量之比为1:8 | |
| B. | 该过程说明Fe(NO3)2溶液不宜加酸酸化 | |
| C. | 每1molNO${\;}_{3}^{-}$发生还原反应,转移6mole- | |
| D. | 若把该反应设计为原电池,则负极反应为Fe2+-e-═Fe3+ |
13.钢铁在锈蚀过程中,下列五种变化:①铁由+2价转化为+3价;②氧气被还原;③产生氢气;④氢氧化铁失水形成Fe2O3•H2O;⑤杂质碳被氧化.可能发生的是( )
| A. | ①② | B. | ③④ | C. | ①②③④ | D. | ①②③④⑤ |
3.下列离子方程式正确的是( )
| A. | 向CaCl2溶液中通入CO2:Ca2++CO2+H2O═CaCO3↓+2H+ | |
| B. | 漂白粉溶液中通入过量SO2:ClOˉ+H2O+SO2═HSO3-+HClO | |
| C. | 在FeSO4溶液中加入H2O2溶液:Fe2++2H2O2+4H+═Fe3++4H2O | |
| D. | 在澄清石灰水中加入少量小苏打溶液:Ca2++OH-+HCO3-═CaCO3↓+H2O |
10.在下列操作中,所使用的仪器能够达到目的是( )
| A. | 用5mL量筒准确量取4.55mL水 | |
| B. | 用分析天平准确地称取6.82g食盐 | |
| C. | 过滤时用玻璃棒搅拌漏斗内的液体,以加速过滤 | |
| D. | 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
7.下列离子方程式正确的是( )
| A. | 碳酸氢钠溶液与少量石灰水反应:HCO3-+OH-+Ca2+═H2O+CaCO3↓ | |
| B. | 氯化铵与氢氧化钠溶液混合:NH4++OH-═H2O+NH3↑ | |
| C. | 向漂白粉溶于水形成的溶液中通入少量的SO2:Ca2++3ClO-+SO2+H2O═CaSO4↓+Cl-+2HClO | |
| D. | 硫化亚铁溶于稀硝酸中:FeS+2H+═Fe2++H2S↑ |
8.下列发展中的化学电源中不属于充电电池的是( )
| A. | 铅蓄电池 | B. | 锂离子电池 | C. | 锌锰电池 | D. | 镍镉电池 |