题目内容
用NA表示阿伏加德罗常数的值.下列叙述正确的是
- A.常温常压下,3.6g D2O中含有的电子总数为2.0NA
- B.标准状况下,11.2LC2H2和N2的混合气分子中叁键数目为0.5NA
- C.常温常压下,4.6g Na在O2中燃烧消耗O2的分子数为0.05NA
- D.25℃时,pH=1的CH3COOH溶液中的H+数为0.1 NA
B
分析:A、依据n= 计算物质的量结合分子式计算电子数;
计算物质的量结合分子式计算电子数;
B、乙炔分子中和氮气分子中都含一个三键,依据n=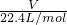 计算物质的量,结合分子式计算三键数;
计算物质的量,结合分子式计算三键数;
C、钠在氧气中燃烧生成过氧化钠,依据化学方程式计算;
D、溶液体积不知,不能计算微粒数;
解答:A、3.6g D2O物质的量= =0.18mol,含有的电子总数为1.8NA,故A错误;
=0.18mol,含有的电子总数为1.8NA,故A错误;
B、标准状况下,11.2LC2H2和N2的混合气体物质的量=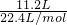 =0.5mol,乙炔分子中和氮气分子中都含一个三键,分子中叁键数目为0.5NA,故B正确;
=0.5mol,乙炔分子中和氮气分子中都含一个三键,分子中叁键数目为0.5NA,故B正确;
C、4.6g Na物质的量为0.2mol,在O2中燃烧生成过氧化钠,2Na+O2=Na2O2,消耗O2的分子数为0.1NA,故C错误;
D、溶液体积不知,不能计算微粒数,故D错误
故选B.
点评:本题考查了阿伏伽德罗常数的应用,主要考查质量换算物质的量计算微粒数,气体摩尔体积的条件应用,题目难度中等.
分析:A、依据n=
 计算物质的量结合分子式计算电子数;
计算物质的量结合分子式计算电子数;B、乙炔分子中和氮气分子中都含一个三键,依据n=
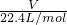 计算物质的量,结合分子式计算三键数;
计算物质的量,结合分子式计算三键数;C、钠在氧气中燃烧生成过氧化钠,依据化学方程式计算;
D、溶液体积不知,不能计算微粒数;
解答:A、3.6g D2O物质的量=
 =0.18mol,含有的电子总数为1.8NA,故A错误;
=0.18mol,含有的电子总数为1.8NA,故A错误;B、标准状况下,11.2LC2H2和N2的混合气体物质的量=
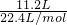 =0.5mol,乙炔分子中和氮气分子中都含一个三键,分子中叁键数目为0.5NA,故B正确;
=0.5mol,乙炔分子中和氮气分子中都含一个三键,分子中叁键数目为0.5NA,故B正确;C、4.6g Na物质的量为0.2mol,在O2中燃烧生成过氧化钠,2Na+O2=Na2O2,消耗O2的分子数为0.1NA,故C错误;
D、溶液体积不知,不能计算微粒数,故D错误
故选B.
点评:本题考查了阿伏伽德罗常数的应用,主要考查质量换算物质的量计算微粒数,气体摩尔体积的条件应用,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目