��Ŀ����
����Ŀ��ʵ�������̷���FeSO47H2O��Ϊ��Դ�Ʊ��������ʰ�������[��NH2 CH2COO��2 Fe�����й��������ʣ�
�ʰ��ᣨNH2CH2COOH�� | ������ | �ʰ������� |
������ˮ�������Ҵ������Ի����� | ������ˮ���Ҵ�����ǿ���Ժͻ�ԭ�� | ������ˮ���������Ҵ� |
ʵ����̣�
I���Ʊ�FeCO3����0.10mol�̷�����ˮ�У������������ۣ��߽����������1.1molL��1NH4HCO3��Һ200mL����Ӧ��������˲�ϴ�ӳ�����
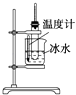
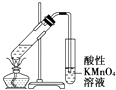
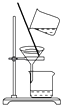
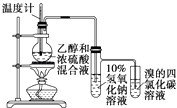
II���Ʊ���NH2 CH2 COO�� 2Fe��ʵ��װ����ͼ���гֺͼ���������ʡ�ԣ�������A�з�Ӧ��C�п����ž����ٽ����������ͺ�0.20mol�ʰ����ˮ��Һ��Ϻ����C�У����������Ტ���ȣ���Ӧ��������ˣ���Һ����Ũ���������Ҵ������ˡ�����õ���Ʒ��
�ش��������⣺
��1��ʵ��I�У����۵������������ɳ��������ӷ���ʽΪ ��
��2��ʵ��II�У�
��װ��B���Լ�Ϊ ��
�ڵ�C�п����ž���Ӧֹͣ�μ����ᣬ��ֹˮ�� �� �ر�ֹˮ��
��װ��D��Ca��OH��2�������� ��
��������ɵ���pH����ϵpH����ʵĹ�ϵ�����
ʵ�� | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
��ϵpH | 4.0 | 4.5 | 5.0 | 5.5 | 6.0 | 6.5 | 7.0 | 7.5 |
����/% | 65.74 | 74.96 | 78.78 | 83.13 | 85.57 | 72.98 | 62.31 | 5686�� |
pH����ʹ�����½���ԭ����������������û���������ţ���
a������Ӧ�յ�ָʾ�� b����ֹ������������ c���ٽ�FeCO3�ܽ� d��������
���Ҵ��������� ��
������Ʒ������Ϊm g�������Ϊ
��3�����ʵ�鷽���ⶨ��Ʒ�ж��������������������������̵�ϸ�ڣ��� ��
����֪��Ʒ�д����������������ҽ����������������������±�KMnO4��NaC1O��H2 O2����������������
���𰸡�
��1����ֹ��������������Fe2++2HCO3��=FeCO3��+CO2��+H2O
��2������NaHCO3��Һ��b��a���ж�װ���п����Ƿ��ž���H+����NH2CH2COOH��Ӧ��bc�����ʰ���������ˮ�е��ܽ�ȣ���߲��ʺʹ��ȣ�![]() ��100%
��100%
��3����ȡһ�������IJ�Ʒ����ˮ�У���������H2SO4�ữ����KMnO4����Һ�ζ�����¼���ĵ�������ظ�ʵ��2��3��
���������⣺��1�����������н�ǿ�Ļ�ԭ�ԣ����Ʊ�̼�������Ĺ����У�Ϊ�˷�ֹ��������������������������ۣ��̷���ˮ��Һ��NH4HCO3��Һ��Ӧ�ķ���ʽΪ Fe2++2HCO3��=FeCO3��+CO2��+H2O�����Դ��ǣ���ֹ��������������Fe2++2HCO3��=FeCO3��+CO2��+H2O����2��������ϡ������ʯ�����Ʊ�������̼�Ĺ����У�HCl�лӷ��ԣ�Ϊ�˱���ӷ�����HCl���ź������飬�����ȥ����ѡ�ñ���NaHCO3��Һ�����Դ��ǣ�����NaHCO3��Һ���ڵ�C�п����ž���Ӧֹͣ�μ����ᣬ�Ʊ�����˹��̲���Ҫ������̼����Ҫ�����������ʲ��ܽ����Ҳ�ķ�Ӧװ�ã���Ӳ�ر�ֹˮ��b����ֹˮ��a�����Դ��ǣ�b��a����װ��D��Ca��OH��2���������ж�װ���п����Ƿ��ž�����������������Ҫ�����������������ʵ����ɸ��ţ����Դ��ǣ��ж�װ���п����Ƿ��ž��� ��pH����ʹ�����½���ԭ����H+����NH2CH2COOH�еİ�����Ӧ����������ǿ���Ժͻ�ԭ�ԣ����û��дٽ�FeCO3�ܽ⣬��ֹ�����������������Դ��ǣ�H+����NH2CH2COOH��Ӧ��bc�������ڸʰ�������������ˮ���������Ҵ������Ҵ��������ǽ��ʰ���������ˮ�е��ܽ�ȣ���߲��ʺʹ��ȣ����Դ��ǣ����ʰ���������ˮ�е��ܽ�ȣ���߲��ʺʹ��ȣ� ����ԭ���غ㣬�̷��е���Ԫ��Ϊ0.10mol��������NH4HCO3��Һ�������ʸ�����ԭ���غ�֪�����ϲ���[��NH2 CH2COO��2 Fe0.10mol��������Ϊ20.4g���ʲ���= ![]() =
= ![]() �����Դ��ǣ�
�����Դ��ǣ� ![]() ����3���ⶨ��Ʒ�ж�������������ȡһ�������IJ�Ʒ����ˮ�У���������H2SO4�ữ����KMnO4����Һ�ζ�����¼���ĵ�������ظ�ʵ��2��3�Σ��ɸ������ĵĸ�����ص���������������������Դ��ǣ���ȡһ�������IJ�Ʒ����ˮ�У���������H2SO4�ữ����KMnO4����Һ�ζ�����¼���ĵ�������ظ�ʵ��2��3�Σ�
����3���ⶨ��Ʒ�ж�������������ȡһ�������IJ�Ʒ����ˮ�У���������H2SO4�ữ����KMnO4����Һ�ζ�����¼���ĵ�������ظ�ʵ��2��3�Σ��ɸ������ĵĸ�����ص���������������������Դ��ǣ���ȡһ�������IJ�Ʒ����ˮ�У���������H2SO4�ữ����KMnO4����Һ�ζ�����¼���ĵ�������ظ�ʵ��2��3�Σ�

 ��У����ϵ�д�
��У����ϵ�д�