题目内容
将10 mol A和5 mol B放入容积为10 L的密闭容器中,某温度下发生反应:3A(g)+B(g) 2C(g),在最初2 s内,消耗A的平均速率为0.06 mol·L-1·s-1,则在2 s时,容器中有 mol A,此时C的物质的量浓度为 。
2C(g),在最初2 s内,消耗A的平均速率为0.06 mol·L-1·s-1,则在2 s时,容器中有 mol A,此时C的物质的量浓度为 。
 2C(g),在最初2 s内,消耗A的平均速率为0.06 mol·L-1·s-1,则在2 s时,容器中有 mol A,此时C的物质的量浓度为 。
2C(g),在最初2 s内,消耗A的平均速率为0.06 mol·L-1·s-1,则在2 s时,容器中有 mol A,此时C的物质的量浓度为 。8.8 0.08 mol·L-1
3A(g) +B(g)  2C(g)
2C(g)
起始浓度(mol·L-1): 1.0 0.5 0
转化浓度(mol·L-1): 0.06×2=0.12 0.04 0.08
2 s时浓度(mol·L-1): 1.0-0.12="0.88" 0.5-0.04="0.46" 0.08
则2 s时,n(A)="0.88" mol·L-1×10 L="8.8" mol,c(C)="0.08" mol·L-1。
 2C(g)
2C(g)起始浓度(mol·L-1): 1.0 0.5 0
转化浓度(mol·L-1): 0.06×2=0.12 0.04 0.08
2 s时浓度(mol·L-1): 1.0-0.12="0.88" 0.5-0.04="0.46" 0.08
则2 s时,n(A)="0.88" mol·L-1×10 L="8.8" mol,c(C)="0.08" mol·L-1。

练习册系列答案
相关题目
 2SO3(g) △H=-190 kJ·mo1-1
2SO3(g) △H=-190 kJ·mo1-1
 Ni(CO)4(g)△H1<0
Ni(CO)4(g)△H1<0 Ni(S)+4CO(g) △H2
Ni(S)+4CO(g) △H2 
 Ni(OH)2+M 电池充电时,阳极的电极反应式为 。电池充电时阴极上发生 (填“氧化”或“还原”)反应
Ni(OH)2+M 电池充电时,阳极的电极反应式为 。电池充电时阴极上发生 (填“氧化”或“还原”)反应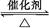 2SO3经一段时间后,SO3的浓度增加了0.4 mol·L-1,在这段时间内用O2表示的反应速率为0.04 mol·(L·s)-1,则这段时间为( )
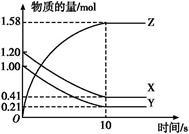
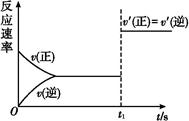
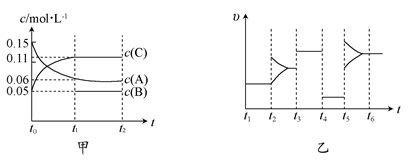
2SO3经一段时间后,SO3的浓度增加了0.4 mol·L-1,在这段时间内用O2表示的反应速率为0.04 mol·(L·s)-1,则这段时间为( ) xC(g) ΔH<0,B、C的物质的量随时间变化的关系如图1,达平衡后在t1、t2、t3、t4时都只改变了一种条件,逆反应速率随时间变化的关系如图2。下列有关说法正确的是( )
xC(g) ΔH<0,B、C的物质的量随时间变化的关系如图1,达平衡后在t1、t2、t3、t4时都只改变了一种条件,逆反应速率随时间变化的关系如图2。下列有关说法正确的是( )

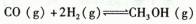



 I3-(aq),其平衡常数表达式为
I3-(aq),其平衡常数表达式为