题目内容
【题目】对下列粒子比较正确的是( )
A. 还原性:F->Cl- B. 粒子半径:Cl->Cl
C. 粒子半径:Na+>Na D. 氧化性:Na+>Al3+
【答案】B
【解析】A.元素的非金属性越强,阴离子的还原性越弱,还原性:F-<Cl-,故A错误;B. 阴离子半径大于对应原子半径,粒子半径:Cl->Cl,故B正确;C.原子或离子电子层数越多其半径越大,Na有3个电子层、钠离子有2个电子层,所以半径:Na+<Na,故C错误;D.元素的金属性越强,阳离子的氧化性越弱,氧化性:Na+<Al3+,故D错误;故选B。

【题目】胆矾是一种常见的化合物,工业上它也是一种制取其它含铜化合物的原料。现有废铜(主要杂质为Fe)来制备胆矾。有人设计了如下流程:
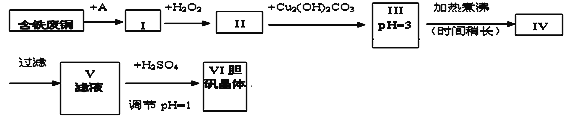
pH值控制可参考下列数据
物 质 | 开始沉淀时的pH值 | 完全沉淀时的pH值 |
氢氧化铁 | 2.7 | 3.7 |
氢氧化亚铁 | 7.6 | 9.6 |
氢氧化铜 | 5.2 | 6.4 |
请根据上述流程回答下列问题:
(1)A物质可选用_____(填字母)。
a.稀H2SO4 b.浓H2SO4/△ c.浓FeCl3溶液 d.浓HNO3
(2)I中加H2O2的离子方程式________________________________________。
(3)II中加Cu2(OH)2CO3的目的是________________________;其优点是__________。
(4)III加热煮沸时发生的化学反应的离子方程式为________________________。
(5)V中加H2SO4调节pH=1是为了____________________________________________。
(6)V到VI的操作是_________________________________
(7)某同学认为上述流程中所加的A物质并不理想,需作改进,其理由是__________。如何改进___________________。



