题目内容
设NA为阿伏加德罗常数,则下列说法正确的是( )
| A.1mol FeCl3形成的 Fe(OH)3胶体中,胶体的颗粒为NA |
| B.标准状况下0.5mol NO和0.5mol O2组成的混合气体的体积约为22.4L |
| C.1molNa2O2与水反应时转移电子数约为NA |
| D.含1molHCl的浓盐酸与足量MnO2反应可制得0.25molCl2 |
C
解析试题分析:A、Fe(OH)3胶体离子为是个Fe(OH)3的集合体,所以1mol FeCl3形成的 Fe(OH)3胶体中,胶体的颗粒小于NA,错误;B、NO与O2发生反应:2NO+O2=2NO2,所以0.5mol NO和0.5mol O2反应生成0.5mol NO,剩余0.25mol O2,则混合气体的体积小于22.4L,错误;C、Na2O2既是氧化剂也是氧化剂,Na2O2反应时电子转移对应关系为:Na2O2 ~ e?,所以1molNa2O2与水反应时转移电子数约为NA,正确;D、随着反应的进行,浓盐酸的浓度逐渐减小,变为稀盐酸后,反应停止,所以含1molHCl的浓盐酸与足量MnO2反应可制得Cl2小于0.25mol,错误。
考点:本题考查阿伏伽德罗常数的应用。

练习册系列答案
相关题目
设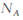 为阿伏加德罗常数的数值,下列说法正确的是
为阿伏加德罗常数的数值,下列说法正确的是
A.标准状况,1molSO3含O原子个数为3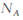 |
B.1.12LN2中含N2分子数为0.05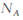 |
C.5.6gFe与足量稀盐酸反应,转移的电子数为0.3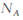 |
D.常温下pH=1的H2SO4溶液中,H+的个数为0.1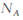 |
同温同压下,aLXm气体和bLYn气体化合,生成cL的化合物z,则z的化学式为( )
| A.XaYb | B.XnYm | C.XamYbn | D. |
下列化学用语正确的是
| A.乙醇的结构简式:C2H6O |
B.CH4的比例模型: |
C.工业上制取粗硅的化学方程式:SiO2+C Si+CO2↑ Si+CO2↑ |
| D.电解饱和食盐水的离子方程式:Cl-+2H2O=Cl2↑+2OH-+H2↑ |
设NA为阿伏伽德罗常数的值。下列说法正确的是
| A.0.1mol丙烯酸中含有双键的数目为0.1NA |
| B.1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA |
| C.标准状况下,11.2L苯中含有分子的数目为0.5NA |
| D.在过氧化钠与水的反应中,每生成0.1mol氧气,转移电子的数目为0.4NA |
NA代表阿伏伽德罗常数。已知C2H4和C3H6的混合物的质量为ag,则该混合物
| A.所含共用电子对数目为(a/7+1)NA | B.所含碳氢键数目为aNA/7 |
| C.燃烧时消耗的O2一定是 33. 6a/ 14L | D.所含原子总数为aNA/14 |
(原创) 下列化学用语使用正确的是
| A.N2的结构式:N = N |
B.H2O的比例模型: |
C.HClO的电子式: |
D.MgBr2的形成过程用电子式表示为: |
设NA为阿伏加德罗常数,下列叙述正确的是
| A.24 g镁的原子最外层电子数为NA |
| B.1 L 0.1mol·L-1乙酸溶液中H+ 数为0.1 NA |
| C.1 mol甲烷分子所含质子数为10 NA |
| D.标准状况下,22.4 L乙醇的分子数为NA |