题目内容
【题目】随着材料科学的发展,金属钒及其化合物得到了越来越广泛的应用,并被誉为“合金维生素”。工业上回收废钒催化剂(含有V2O5、VOSO4及不溶性残渣),科研人员最新研制了一种离子交换法回收钒的新工艺,回收率达91.7%以上。该工艺的主要流程如图所示:
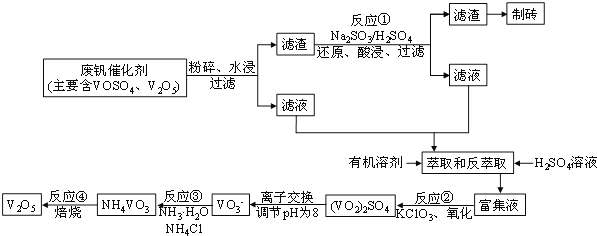
已知部分含钒物质在水中的溶解性如下表所示:
物质 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 |
溶解性 | 可溶 | 难溶 | 难溶 | 易溶 |
请问答下列问题:
(1)工业上由V2O5冶炼金属钒常用铝热剂法,其化学方程式可表示为____。
(2)滤液中含钒的主要成分________(写化学式)。反应①的离子方程式___________________。
(3)萃取和反萃取过程中所需的主要玻璃仪器为_____________。若反萃取使用硫酸用量过大,进一步处理会增加_______(填化学式)的用量,造成成本增大。
(4)该工艺反应③的沉淀率(又称沉钒率)是回收钒的关键之一,写出该步发生反应的离子方程式___________________。“沉淀”过程中,沉钒率受温度、氯化铵系数(NH4Cl的质量与调节pH之后的料液中VO3-的质量比)等的影响,其中温度与沉钒率的关系如图所示,温度高于80℃沉钒率降低的可能原因是___________________________。

(5)25℃时,取样进行试验分析,得到钒沉淀率和溶液pH之间关系如下表:
pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
钒沉淀率% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.8 | 96.4 | 93.1 | 89.3 |
结合上表,在实际生产中,③中加入氨水,调节溶液的最佳pH值为____。若矾沉淀率为93.1%时不产生Fe(OH)3沉淀,则溶液中c(Fe3+)<_____。(已知:25℃时,Ksp[Fe(OH)3]=2.6×10-39)
(6)废钒催化剂中V2O5的质量分数为6%(原料中的所有钒已换算成V2O5)。取100g此废钒催化剂按上述流程进行实验,当加入105mL 0.1molL-1的KClO3溶液时,溶液中的钒恰好被完全处理,假设以后各步钒没有损失,则该工业生产中钒的回收率是______________。
【答案】 3V2O5 + 10Al![]() 6V + 5Al2O3 VOSO4 V2O5 + SO32- + 4H+ = 2V02+ +SO42- +2H2O 分液漏斗 NH3·H2O NH4+ + VO3- = NH4VO3 ↓ 温度高于80℃,导致部分氯化铵分解 1.7~1.8 2.6×10-3mol/L 95.55%
6V + 5Al2O3 VOSO4 V2O5 + SO32- + 4H+ = 2V02+ +SO42- +2H2O 分液漏斗 NH3·H2O NH4+ + VO3- = NH4VO3 ↓ 温度高于80℃,导致部分氯化铵分解 1.7~1.8 2.6×10-3mol/L 95.55%
【解析】(1)铝与五氧化二钒反应生成钒与氧化铝,反应方程式为![]()
(2)因为VOSO4可溶,V2O5难溶,所以滤液中含钒的主要成分VOSO4。V2O5具有氧化性,Na2SO3具有还原性,所以反应①的离子方程式V2O5 + SO32- + 4H+ = 2V02+ +SO42- +2H2O。
(3)萃取和反萃取过程中所需的主要玻璃仪器为分液漏斗。若反萃取使用硫酸用量过大,进一步处理会增加NH3·H2O的用量,造成成本增大
(4)因为反应③为 NH4VO3为难溶性物质,所以该步发生反应的离子方程式NH4++ VO3-=NH4VO3。由图分析80℃之前沉钒率逐渐升高。80℃之后因为氯化铵受热分解了,导致NH4+离子浓度降低了,所以沉钒率逐渐减小。答案:NH4+ + VO3-=NH4VO3,温度高于80℃,导致部分氯化铵分解。
NH4VO3为难溶性物质,所以该步发生反应的离子方程式NH4++ VO3-=NH4VO3。由图分析80℃之前沉钒率逐渐升高。80℃之后因为氯化铵受热分解了,导致NH4+离子浓度降低了,所以沉钒率逐渐减小。答案:NH4+ + VO3-=NH4VO3,温度高于80℃,导致部分氯化铵分解。
根据表中数据判断,(5)中加入氨水,调节溶液pH最佳值为1.7-1.8(或1.7、1.8其中一个),此时钡沉淀率达到最大,需要调节的PH较小;若钒沉淀率为93.1%,时不产生Fe(OH)3沉淀,此时PH=2,氢离子浓度=10-2 mol/L ,c(OH-)=10-12 mol/L,则溶液中才c(Fe3+)浓度根据溶度积计算Ksp[Fe(OH)3]=c(Fe3+). c3 (OH-)=2.6×10-39,,计算得到c(Fe3+)=2.6×10-3 mol/L,不产生Fe(OH)3沉淀,则溶液中c(Fe3+)<4.0×10-2 mol/L.,因此,本题正确答案是: 1.7-1.8 (或1.7、1.8其中一个);2.6×10-3mol/L.。
(6)根据题意V2O5+SO32-+4H+ =2V02++SO42-+2H2O,V02+被ClO3-氧化,由ClO3-+6 V02++6H+=6VO3++Cl-+3H2O ,可知
3V2O5~-6V02+~ClO3-
3mol 1mol
n 0.0105mol
解得n=0.0315mol,因此该实验中钒的回收率=[(0.0315mol×182g/mol )/(100g×6%.)]×100%=95.55%。

 应用题作业本系列答案
应用题作业本系列答案 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案