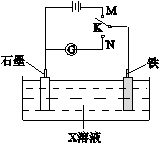
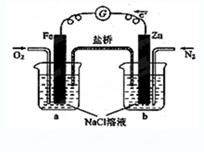
题目内容
某种氢氧燃料电池的电解液为KOH溶液,下列有关该电池的叙述不正确的是( )
| A.正极反应式为:O2+2H2O+4e-=4OH- |
| B.工作一段时间后,电解液中KOH的物质的量不变 |
| C.该燃料电池的总反应方程式为:2H2+O2=2H2O |
| D.用该电池电解CuCl2溶液,产生2.24 L Cl2(标准状况)时,有0.1 mol电子转移 |
D
把释放能量的氧化还原反应:2H2+O2=2H2O通过电池反应进行就制得氢氧燃料电池。H2失去电子,在负极上被氧化,产生H+,由于电解液中有大量的OH-,所以电极反应式为:2H2-4e-+4OH-=4H2O。工作一段时间后,KOH溶液被稀释,但KOH的物质的量不变。D项,n(Cl2)=0.1 mol,转移电子0.2 mol。

练习册系列答案
相关题目


 (填“从左向右”“从右向左”或“不”)移动;滤纸上能观察到的现象有 。
(填“从左向右”“从右向左”或“不”)移动;滤纸上能观察到的现象有 。  )在溶液中呈紫红色。
)在溶液中呈紫红色。
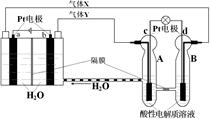
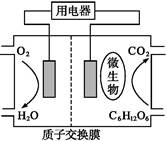
 6CO2↑+24H+
6CO2↑+24H+