题目内容
如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。据此回答下列问题:

(1)该硫酸的物质的量浓度为 mol/L。
(2)配制250mL 0.92mol·L-1的稀硫酸需取该硫酸 mL。(2分)
(3)配制时必需的玻璃仪器有:______________________________________________________。(2分)
(4)定容时,待容量瓶中溶液的凹液面正好与刻度线相切,盖好瓶塞后的下一步操作是______。(1分)
(5)定容时,若加入的水超过刻度线,必须采取的措施是 。(1分)
(6)下列操作对H2SO4的物质的量浓度有什么影响(偏高、偏低或无影响)?
①转移溶液后,未洗涤烧杯: ;(1分)
②容量瓶用水洗净后未烘干: ;(1分)
③定容时俯视容量瓶的刻度线: 。(1分)
(1)18.4mol/L(2分) (2)12.5mL(2分)
(3)烧杯,玻璃棒,250ml容量瓶,胶头滴管,量筒(2分)
(4)倒转摇匀(1分) (5)重新配制(1分) (6)①偏低(1分)②无影响(1分)③偏高(1分)
【解析】
试题分析:(1)根据c=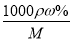 可知,该硫酸的物质的量浓度为c=
可知,该硫酸的物质的量浓度为c=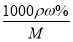 =
=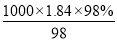 =18.4mol/L。
=18.4mol/L。
(2)在稀释过程中溶质的物质的量是不变的,则配制250mL 0.92mol·L-1的稀硫酸需取该硫酸的体积=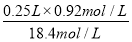 =0.0125L=12.5ml。
=0.0125L=12.5ml。
(3)浓硫酸需要量筒量取,浓硫酸的稀释需要烧杯和玻璃棒,定容还需要胶头滴管,所以配制一定物质的量浓度溶液时必需的玻璃仪器有烧杯,玻璃棒,250ml容量瓶,胶头滴管,量筒。
(4)定容时,待容量瓶中溶液的凹液面正好与刻度线相切,盖好瓶塞后的下一步操作是倒转摇匀。
(5)定容时,若加入的水超过刻度线,这说明实验失败,必须采取的措施是重新配制。
(6)根据cB=nB/V可得,一定物质的量浓度溶液配制的误差都是由溶质的物质的量nB和溶液的体积V引起的。误差分析时,关键要看配制过程中引起n和V怎样的变化。在配制一定物质的量浓度溶液时,若nB比理论值小,或V比理论值大时,都会使所配溶液浓度偏小;若nB比理论值大,或V比理论值小时,都会使所配溶液浓度偏大。①转移溶液后,未洗涤烧杯,则溶质减少,所配浓度偏低;②容量瓶用水洗净后未烘干,则溶液体积和溶质质量均不变,因此所配浓度无影响;③定容时俯视容量瓶的刻度线,则容量瓶中溶液的体积减少,因此所配浓度偏高。
考点:考查物质的量浓度的计算、配制以及误差分析等

 阅读快车系列答案
阅读快车系列答案