题目内容
【题目】如图所示,下列说法不正确的是( )
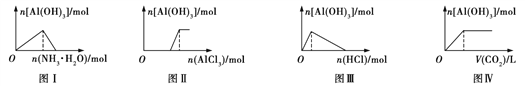
A. 图Ⅱ表示向NaOH溶液中滴加AlCl3溶液至过量且边滴边振荡
B. 图Ⅰ表示向AlCl3溶液中滴加氨水至过量
C. 图Ⅲ表示向NaAlO2溶液中滴加稀盐酸至过量且边滴边振荡
D. 图Ⅳ表示向NaAlO2溶液中缓慢通入二氧化碳至过量
【答案】B
【解析】A、设AlCl3为1mol,产生1molAl(OH)3时消耗3mol的NaOH,再加NaOH,发生Al(OH)3+NaOH=NaAlO2+2H2O,消耗1molNaOH,所以沉淀量最大前后NaOH的物质的量之比为3:1,选项A正确;B、向饱和AlCl3溶液中滴加氨水至过量,反应生成氢氧化铝沉淀和氯化铵,反应的离子方程式为:Al3++3NH3·H2O═Al(OH)3↓+3NH4+,反应一开始就产生沉淀且沉淀不溶于过量氨水,选项B错误;C、向NaAlO2溶液中滴加稀盐酸,开始阶段先产生氢氧化铝沉淀,发生反应:AlO2-+H++H2O=Al(OH)3↓,随着盐酸的逐滴加入,则沉淀开始溶解,发生反应:Al(OH)3+3H+=Al3++3H2O,所以沉淀量达到最大消耗的盐酸和沉淀完全溶解消耗的盐酸的物质的量之比是1:3,选项C正确;D、向NaAlO2溶液中缓慢通入二氧化碳至过量,发生的离子反应为AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,生成的沉淀不溶于过量的碳酸,后阶段沉淀的量不变,选项D正确。答案选B。

 金状元绩优好卷系列答案
金状元绩优好卷系列答案【题目】表中,第Ⅰ栏和第Ⅱ栏的化学反应都可以用第Ⅲ栏的离子方程式表示的是( )
编号 | 第Ⅰ栏 | 第Ⅱ栏 | 第Ⅲ栏 |
A | H2SO4溶液中滴加Ba(OH)2至恰好沉淀完全 | 在NaHSO4溶液中滴加Ba(OH)2至中性 | H++SO |
B | 氢氧化钠溶液中通入过量CO2 | 氢氧化钙溶液中滴入过量CO2 | OH﹣+CO2═HCO |
C | 向碳酸氢铵溶液中加过量澄清石灰水 | 向碳酸氢钠溶液中加过量澄清石灰水 | HCO |
D | FeBr2溶液和少量Cl2反应 | FeI2溶液和少量Cl2反应 | 2Fe2++Cl2═2Fe3++2Cl﹣ |
A.A
B.B
C.C
D.D