题目内容
6.钛(Ti)被称为继铁,铝之后的第三金属,其合金广泛用于航天工业,称为21世纪钢铁.我国钛铁矿储量居世界首位,现以含杂质的钛铁矿(主要成份为FeTiO3)制取Ti的流程如下: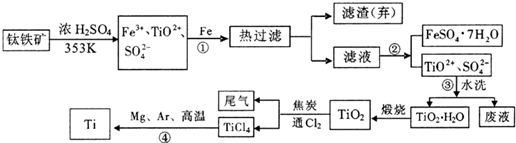
回答下列问题:
(1)Ti的原子序数为22,它位于元素周期表中第四周期ⅣB族.
(2)上述制备Ti的过程中,可以利用的副产物是FeSO4•7H2O;考虑成本和废物综合利用因素,废液中可加入石灰(或碳酸钙、废碱)处理.
(3)已知①C(s)+O2(g)=CO2(g);△H=-393.5kJ•mol-1
②2CO(g)+O2(g)=2CO2(g);△H=-566kJ•mol-1
③TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g);△H=+141kJ•mol-1
则TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的△H=-80kJ•mol-1.
(4)反应④在Ar气氛中进行的理由是防止高温下Mg(Ti)与空气中的O2(或CO2、N2)作用.
(5)实验室取该矿石19.00克,通过上述流程,最终得到5.00g含镁4%的钛镁合金.假设实验室或工业生产中钛铁矿中杂质是不与浓H2SO4反应的固体,生产过程中钛的损失忽略不计,反应①过程中无气体产生,则工业使用该钛铁矿制得含镁4%的合金25.0吨,理论上最多可获得副产品FeSO4•7H2O是139吨.
分析 铁粉的作用由步骤①的前后以及最后所得产物中的FeSO4•7H2O分析,不难得出是为了除去混合溶液中的Fe3+,趁热过滤得热的FeSO4溶液,步骤②为冷却,可得FeSO4•7H2O晶体,滤液水洗后得TiO2•H2O,煅烧得TiO2,TiO2与碳、氯气在高温下反应得TiCl4和CO,用镁还原TiCl4得Ti,据此答题.
解答 解:铁粉的作用由步骤①的前后以及最后所得产物中的FeSO4•7H2O分析,不难得出是为了除去混合溶液中的Fe3+,趁热过滤得热的FeSO4溶液,步骤②为冷却,可得FeSO4•7H2O晶体,滤液水洗后得TiO2•H2O,煅烧得TiO2,TiO2与碳、氯气在高温下反应得TiCl4和CO,用镁还原TiCl4得Ti,
(1)Ti位于元素周期表中第四周期ⅣB族,
故答案为:四;ⅣB;
(2)根据上面的分析可知,可以利用的副产物是FeSO4•7H2O,图示水浸过程生成H2TiO3同时生成的H2SO4溶液(TiOSO4+2H2O=H2TiO3+H2SO4),应加入碱性物质处理,可以是石灰(或碳酸钙、废碱),
故答案为:FeSO4•7H2O; 石灰(或碳酸钙、废碱);
(3)依盖斯定律,将③+①×2-②可得:TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g),△H=(+141kJ•mol-1)+2×(-393.5kJ•mol-1)-(-566kJ•mol-1)=-80 kJ•mol-1,
故答案为:-80 kJ•mol-1;
(4)Mg是活泼金属,能与空气中多种物质反应,因此可得出Ar气作用为保护气,防止Mg和空气中物质反应,
故答案为:防止高温下Mg(Ti)与空气中的O2(或CO2、N2)作用;
(5)实验室取该矿石19.00克,通过上述流程,最终得到5.00g含镁4%的钛镁合金,合金中钛的质量为4.8g,根据钛铁矿(主要成份为FeTiO3)可知,矿石中钛与铁的物质的量之比为1:1,所以制得含镁4%的合金25.0吨,可得钛24吨,即钛的物质的量为$\frac{24×1{0}^{6}}{48}$mol=5×105mol,根据元素守恒,FeSO4•7H2O的物质的量与钛相等,所以FeSO4•7H2O的质量为5×105×278g=139吨,
故答案为:139.
点评 本题考查学生对工艺流程理解、阅读题目获取信息能力、氧化还原反应及方程式的书写等,难度中等,理解工艺流程是关键,需要学生具有阅读题目获取信息能力和灵活运用基础知识分析问题、解决问题能力.

 活力课时同步练习册系列答案
活力课时同步练习册系列答案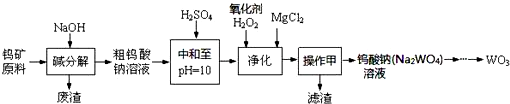
回答下列问题:
(1)上述流程中操作甲的名称是过滤.
(2)钨矿原料“碱分解”时的浸出率与原料中的CaO含量、NaOH浓度、碱用量等都有关系,如下表所示.下列说法正确的是A.
钨矿原料碱分解时的浸出率受NaOH浓度等因素影响的关系图
| w(CaO)% NaOH浓度& 浸出率% 碱用量c/mol•L-1 | 0.1 | 1.3 | 1.3 | 2.7 |
| 30 | 30 | 40 | 40 | |
| 1.1 | 99.1 | 90.1 | 93.3 | 83.2 |
| 1.3 | 99.4 | 92.7 | 93.0 | 82.1 |
| 1.5 | 99.5 | 93.4 | 96.5 | 83.0 |
A.增大NaOH浓度浸出率增大 B.增大碱用量浸出率一定增大
C.增大碱用量浸出率一定减小 D.原料中CaO的含量增大则浸出率增大
(3)pH=10的溶液中含有的杂质阴离子有SiO32-、HAsO32-、HAsO42-、HPO42-等.则“净化”时,加入H2O2反应的离子方程式HAsO32-+H2O2=HAsO42-+H2O.
(4)在“净化”阶段,若常温下所得溶液pH=9.5,为不产生Mg(OH)2沉淀,溶液中c(Mg2+)应不超过5.6×10-3mol•L-1.[Ksp(Mg(OH)2=5.6×10-12]
(5)上述流程中所得的产品质量较好,但有废物排出,排出的废水中含有的主要物质是Na2SO4、NaCl(填化学式).
(6)用酸性介质中的碳化钨(WC)的阳极氧化法,可以从碳化钨废料中回收钨.电解时,用碳化钨做阳极,不锈钢做阴极,阳极析出钨酸并放出无污染的气体.该阳极反应式为WC+6H2O-10e-=H2WO4+CO2↑+10H+.
| A. | 汽车轮胎 | B. | 涤纶 | C. | 聚乙烯制品 | D. | 玻璃钢 |
| A | B | C | D | |
| 容量瓶规格 | 1000mL | 950mL | 500mL | 1000mL |
| CuSO4质量 | 152g | 152g | 80g | 160g |
| A. | A | B. | B | C. | C | D. | D |
| A. | Ca(OH)2+CO2═CaCO3+H2O | B. | Na2O+H2O═2NaOH | ||
| C. | 2Na2O2+2H2O═4NaOH+O2 | D. | 2NaHCO3═Na2CO3+CO2+H2O |

