题目内容
【题目】25 ℃时,对于pH=2的CH3COOH溶液,下列判断正确的是( )
A. 加水稀释,电离平衡正向移动,溶液中c(H+)增大,![]() 也增大
也增大
B. 通入少量HCl气体,电离平衡逆向移动,c(CH3COO-)减小,Ka减小
C. 加入少量CH3COONa固体,电离平衡逆向移动,c(H+)减小,Ka不变
D. 升高温度,电离平衡正向移动,c(H+)增大,pH增大
【答案】C
【解析】A项,加水稀释,促进醋酸电离,电离平衡正向移动,但根据化学平衡移动原理(电离平衡也适用),溶液中c(H+)减小, 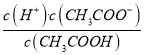 =Ka,温度一定时Ka是常数,故A错误;B项,通入少量HCl气体,c(H+)增大,根据化学平衡移动原理,电离平衡逆向移动,c(CH3COO-)减小,但温度一定时Ka是常数,故B错误;C项,加入少量CH3COONa固体,c(CH3COO-)增大,根据化学平衡移动原理,CH3COOH电离平衡逆向移动,c(H+)减小,因为温度没变,所以Ka不变,故C正确;D项,CH3COOH的电离是吸热过程,升高温度,电离平衡正向移动,c(H+)增大,pH减小,故D错误。
=Ka,温度一定时Ka是常数,故A错误;B项,通入少量HCl气体,c(H+)增大,根据化学平衡移动原理,电离平衡逆向移动,c(CH3COO-)减小,但温度一定时Ka是常数,故B错误;C项,加入少量CH3COONa固体,c(CH3COO-)增大,根据化学平衡移动原理,CH3COOH电离平衡逆向移动,c(H+)减小,因为温度没变,所以Ka不变,故C正确;D项,CH3COOH的电离是吸热过程,升高温度,电离平衡正向移动,c(H+)增大,pH减小,故D错误。

【题目】H2O2广泛应用于医疗卫生、化学合成等领域。
(1)H2O2的电子式是___________。
(2)趣味实验“大象牙膏”的实验原理是H2O2溶液在KI催化作用下分解,反应的机理可表示为:i.H2O2(l)+I-(aq)==== H2O(l)+IO-(aq) △H1 = +a kJ/moL(a > 0)
ii.H2O2(l)+________________________________。
① 2H2O2(l)=2H2O(l)+O2(g) △H=-196kJ/mol,补全反应ii_______________(用热化学方程式表示)。
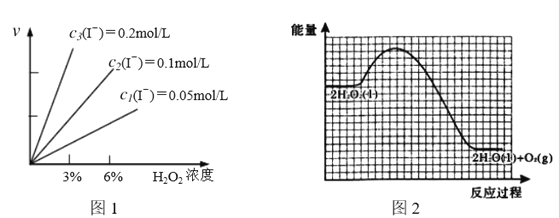
② 某小组在研究影响H2O2分解速率的因素时得到图1的数据关系,由此得出的结论是________。
③ 已知:i的反应速率小于ii的反应速率,在图2画出H2O2溶液中加入KI后,“反应过程—能量”示意图。_________
(3)为分析不同试剂是否对H2O2分解有催化作用,该小组向四支盛有10mL5% H2O2的试管中滴加不同溶液,实验记录如下:
试管 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
滴加试剂 | 2滴1mol/L NaCl | 2滴1mol/L CuSO4 | 2滴1mol/L CuSO4 和2滴1mol/L NaCl | 2滴1mol/L CuSO4 和4滴1mol/L NaCl |
产生气泡情况 | 无气泡产生 | 均产生气泡,且气泡速率从Ⅱ到Ⅳ依次加快 | ||
实验Ⅰ的目的是______________,由实验(3)可得出的结论是________________。