题目内容
【题目】化学与生活密切相关。下列叙述错误的是( )
A.高纯硅可用于制作光感电池B.铝合金大量用于高铁建设
C.活性炭具有除异味和杀菌作用D.冬季燃煤中掺石灰可降低SO2排放
【答案】C
【解析】
A项、硅是一种良好的半导体材料,则高纯硅可用于制作光感电池,故A正确;
B项、铝合金密度低,但强度比较高,接近或超过优质钢,塑性好,可加工成各种型材,具有优良的导电性、导热性和抗蚀性,大量用于高铁建设,故B正确;
C项、活性炭具有很强的吸附性,可以除异味,但不能起杀菌作用,故C错误;
D项、燃煤中掺石灰,氧化钙能与煤燃烧生成的二氧化硫反应生成亚硫酸钙,亚硫酸钙与氧气反应生成硫酸钙,从而减少二氧化硫排放,故D正确;
故选C。

【题目】为探究氮的化合物相关性质,设计了如下实验,请你一起完成相关的探究过程。
(1)将一定量的氨气通入水中并配成1.00L溶液,取20.00mL的该溶液与0.100mol/L的HCl溶液进行中和滴定,为了准确判定终点,应在锥形瓶中加入2-3滴________作指示剂,滴定结果如下表:
实验次数 | 氨水用量(mL) | 盐酸初始读数(mL) | 盐酸最终读数(mL) |
第1次实验 | 20.00 | 0 | 20.10 |
第2次实验 | 20.00 | 1.10 | 21.00 |
第3次实验 | 20.00 | 0.20 | 22.20 |
根据以上滴定结果,测得氨水的物质的量浓度是_________,恰好中和时溶液呈____性(填“酸”或“碱”),用离子方程式解释其原因_______________________________________。
(2)如将干燥的氨气通入装有灼热氧化铜的玻璃管,发生反应生成两种单质,试写出该反应的化学方程式:___________________________________________。该反应中氨气表现出__________性 (填“氧化”或“还原”)
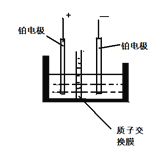
(3)NH4NO3是农业生产中常用的一种化肥,但大量使用易造成水体中氮含量超标而导致水体富营养化,使水体发黑发臭,现用如图装置对水中的铵根及硝酸根进行处理形成无污染的物质。NO3-在______(填 “阴极”或“阳极”或“正极”或“负极”)反应,该电极反应方程式为:___________________________________。