题目内容
(14分)工业上利用CO和水蒸气在一定条件下发生反应制取氢气:
CO(g)+H2O(g)  CO2(g)+H2(g) △H=-41 kJ/mol
CO2(g)+H2(g) △H=-41 kJ/mol
某小组研究在相同温度下该反应过程中的能量变化。他们分别在体积均为V L的两个恒温恒容密闭容器中加入一定量的反应物,使其在相同温度下发生反应。相关数据如下:
|
容器编号 |
起始时各物质物质的量/mol |
达到平衡的时间/min |
达平衡时体系能量的变化/kJ |
||||
|
CO |
H2O |
CO2 |
H2 |
||||
|
① |
1 |
4 |
0 |
0 |
t1 |
放出热量:32.8 kJ |
|
|
② |
2 |
8 |
0 |
0 |
t2 |
放出热量:Q |
|
(1)该反应过程中,反应物分子化学键断裂时所吸收的总能量 (填“大于”、“小于”或“等于”)生成物分子化学键形成时所释放的总能量。
(2)容器①中反应达平衡时,CO的转化率为 %。
(3)计算容器②中反应的平衡常数K= 。
(4)下列叙述正确的是 (填字母序号)。
a.平衡时,两容器中H2的体积分数相等
b.容器②中反应达平衡状态时,Q > 65.6 kJ
c.反应开始时,两容器中反应的化学反应速率相等
d.容器①中,反应的化学反应速率为:
(5)已知:2H2 (g) + O2 (g) ="=" 2H2O (g) ΔH=-484 kJ/mol,写出CO完全燃烧生成CO2的热化学方程式: 。
(6)容器①中反应进行到t min时,测得混合气体中CO2的物质的量为0.6 mol。若用
200 mL 5 mol/L的NaOH溶液将其完全吸收,反应的离子方程式为(用一个离子方程式表示) 。
(1)小于(答“<”不扣分) (2)80 (3)1 (4)a
(5)2CO(g) + O2(g) ="==" 2CO2(g) △H =" -566" kJ/mol
(6)3CO2 + 5OH- ="==" 2CO32- + HCO3- + 2H2O
【解析】
试题分析:(1)该反应是放热反应,反应物分子化学键断裂时所吸收的总能量小于生成物分子化学键形成时所释放的总能量。
(2)容器①中反应达平衡时,放出热量为32.8 kJ,因为1molCO完全转化时放出热量是41 kJ,说明转化的CO为32.8/41=0.8,即CO的转化率为80%。
(3)因为温度没有变化,容器②与容器①中反应的平衡常数完全一样,容器①中反应的平衡常数为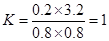 ,即容器②中K=1。
,即容器②中K=1。
(4)因为两个平衡的温度相同,加入的量成比例,达到平衡时各物质的量也成比例增加,两容器中H2的体积分数相等;容器②中反应达平衡状态时,放出的热量是容器①的2倍,Q ="65.6"
kJ;容器②的浓度大,化学反应速率要大;容器①中,反应的化学反应速率应该是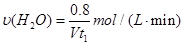 。
。
(5)CO(g)+H2O(g)  CO2(g)+H2(g);△H=-41 kJ/mol为①,2H2 (g) + O2
(g) ="=" 2H2O (g);ΔH=-484 kJ/mol为②,①×2+②即可以达到方程式2CO(g) + O2(g)
="==" 2CO2(g);△H ="
-566" kJ/mol。
CO2(g)+H2(g);△H=-41 kJ/mol为①,2H2 (g) + O2
(g) ="=" 2H2O (g);ΔH=-484 kJ/mol为②,①×2+②即可以达到方程式2CO(g) + O2(g)
="==" 2CO2(g);△H ="
-566" kJ/mol。
(6)CO2的物质的量为0.6 mol,1 mol的NaOH溶液与其完全反应,则产物有CO32-、 HCO3-。根据反应物的物质的量之比可以写出方程式为3CO2 + 5OH- ="==" 2CO32- + HCO3- + 2H2O。
考点:考查化学平衡状态、平衡的移动、速率的计算、化学平衡常数的计算、及热化学方程式的书写与计算。
点评:本题以制取氢气为载体,着重考查化学反应速率、化学平衡及热化学方程式等理论知识,综合性较强,属于难度较大的习题。

 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案