题目内容
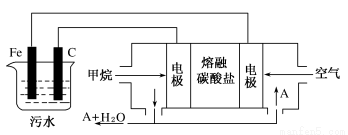
如下图所示,图Ⅰ是恒压密闭容器,图Ⅱ是恒容密闭容器。当其它条件相同时,在Ⅰ、Ⅱ中分别加入2 mol X和2 mol Y,开始时容器的体积均为V L,发生如下反应并达到平衡状态: 2X(?)+Y(?) aZ(g)。此时Ⅰ中X、Y、Z的物质的量之比为1∶3∶2。下列判断正确的是( )
aZ(g)。此时Ⅰ中X、Y、Z的物质的量之比为1∶3∶2。下列判断正确的是( )

A.物质Z的化学计量数a = 2
B.若Ⅱ中气体的密度如图Ⅲ所示,则X、Y中只有一种为气态
C.若X、Y均为气态,则在平衡时X的转化率:Ⅰ﹤Ⅱ
D.若X为固态、Y为气态,则Ⅰ、Ⅱ中从开始到平衡所需的时间:Ⅰ>Ⅱ
B
【解析】
试题分析:A、设达平衡时Y反应的物质的量为x,则:
2X(?)+Y(?)?a Z(g)
起始量:2 2 0
转化量:2x x ax
平衡量:2﹣2x 2﹣x ax
由(2﹣2x):(2﹣x):ax=1:3:2可得x=0.8,a=1,故A错误;
B.如X、Y都是气体,则混合气体的密度不变,如图所示,体积不变,气体的密度增大,则应有固体或液体参加反应生成气体,则X、Y中只有一种为气态,故B正确;C.若X、Y均为气态,反应Ⅰ体系的压强大于反应Ⅱ体系的压强,反应Ⅰ可看成是在Ⅱ的基础上增大压强,平衡向反应方向移动,则转化率Ⅰ>Ⅱ,故C错误;D.若X为固态、Y为气态,则反应前后气体的物质的量相等,压强不变,图Ⅱ压强等于图Ⅰ压强,则Ⅰ、Ⅱ中从开始到平衡所需的时间:Ⅰ=Ⅱ,故D错误;故选B。
考点:本题考查化学平衡的计算,明确物质的状态及压强对平衡移动的影响即可解答,注意两种状态可固定一种状态来分析另一种状态。

 阅读快车系列答案
阅读快车系列答案四个体积相同的密闭容器中在一定的条件下发生反应: 2SO2+O2  2SO3,反应开始时,反应速率由大到小排列顺序正确的是
2SO3,反应开始时,反应速率由大到小排列顺序正确的是
容器 | 温度 | SO2(mol) | O2(mol) | 催化剂 |
甲 | 500℃ | 10 | 5 | - |
乙 | 500℃ | 10 | 5 | V2O5 |
丙 | 450℃ | 8 | 5 | - |
丁 | 500℃ | 8 | 5 | - |
A.乙>甲>丁>丙 B.乙>甲>丙>丁 C.甲>乙=丁>丙 D.乙>甲>丙=丁
实验室用少量的溴水和足量的乙醇制备1,2—二溴乙烷的装置如下图所示:
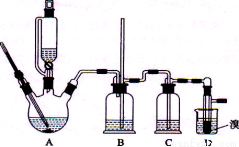
有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g · cm-3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | -l30 | 9 | -1l6 |
回答下列问题:
(1) 烧瓶A中发生的主要的反应方程式: 。
(2) 安全瓶B可以防倒吸,并可以检查实验进行时试管D是否发生堵塞。请写出发生堵塞时瓶B中的现象: 。
(3) 在装置C中应加入 (填字母) ,其目的是
a.水 b.浓硫酸 c.氢氧化钠溶液
(4)若产物中有少量未反应的Br2,最好用 洗涤除去。(填字母)
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
(5)若产物中有少量副产物乙醚,可用 的方法除去。
(6)反应过程中应用冷水冷却装置D,但又不能过度冷却(如用冰水),其原因是 。