题目内容
【题目】I.一密封体系中发生下列反应:N2+3H2![]() 2NH3 ΔH<0,下图是某一时间段中反应速率与反应进程的曲线关系图:
2NH3 ΔH<0,下图是某一时间段中反应速率与反应进程的曲线关系图:
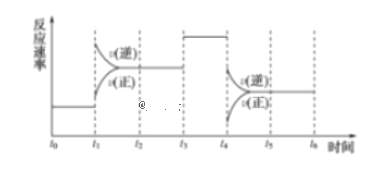
回答下列问题:
(1)处于平衡状态的时间段是___________、___________、___________。
(2)t1、t3、t4时刻体系中分别是什么条件发生了变化:____________、___________、___________。
(3)下列各时间段时,氨的百分含量最高的是___________(填序号)。
A.t0~t1 B.t2~t3 C.t3~t4 D.t5~t6
II.830K时,在密闭容器中发生下列可逆反应:CO(g)+H2O(g)![]() CO2(g)+H2(g)△H<0。试回答下列问题:
CO2(g)+H2(g)△H<0。试回答下列问题:
(4)若起始时c(CO)=2mol·L-1,c(H2O)=3mol·L-1,达到平衡时CO的转化率为60%,则在该温度下,该反应的平衡常数K=____________。
(5)在相同温度下,若起始时c(CO)=1mol·L-1,c(H2O)=2mol·L-1,反应进行一段时间后,测得H2的浓度为0.5mol·L-1,则此时该反应是否达到平衡状态______(填“是”与“否”),此时v(正)____v(逆)(填“大于”“小于”或“等于”)。
【答案】t0~t1 t2~t4 t5~t6 升高温度 加催化剂 降低压强 A 1 否 大于
【解析】
(1)从平衡状态的本质特征分析,可逆反应达到平衡时,正逆反应速率相等;
(2)根据温度、催化剂以及压强对反应速率的影响分析,注意各时间段正逆反应速率的变化;
(3)随着反应的进行,生成的氨气逐渐增多,氨气的体积分数逐渐增大;
(4)根据三段式解题法,求出反应混合物各组分浓度的变化量、平衡时各组分的浓度,代入平衡常数表达式计算平衡常数;
(5)计算常数的浓度商Qc、平衡常数,与平衡常数比较判断反应进行方向,据此解答。
(1)从平衡状态的本质特征分析,可逆反应达到平衡时,正逆反应速率相等,时间处于t0~t1,t2~t3,t3~t4,t5~t6时,正逆反应速率相等,则说明反应达到平衡状态,
故答案为:t0~t1,t2~t4,t5~t6;
(2)t1时,正逆反应速率都增大,且逆反应速率大于正反应速率,平衡向逆反应方向移动,由反应方程式△H<0可知,应为升高温度;t3时,正逆反应速率都增大并且相等,平衡不移动,应为加入催化剂的变化;t4时,正逆反应速率都减小,且逆反应速率大于正反应速率,平衡向逆反应方向移动,由方程式计量数关系可知,应为减小压强的变化;
故答案为:升高温度;加催化剂;降低压强;
(3)随着反应的进行,生成的氨气逐渐增多,氨气的体积分数逐渐增大,反应进行到最大时间时,生成的氨气最多,氨的体积分数最高,由于t1~t2时间段和t4~t5时间段内,平衡都向逆反应方向移动,氨的百分含量都减小,所以应是t0~t1时间段中氨的百分含量最高,
故答案为:A;
(4)平衡时CO的转化率为60%,则CO的浓度变化量=2mol/L×60%=1.2mol/L,则:

故平衡常数![]() ,
,
故答案为:1;
(5)在相同温度下(850℃),若起始时c(CO)=1molL1,c(H2O)=2molL1,反应进行一段时间后,测得H2的浓度为0.5molL1,则:

浓度商![]() ,故平衡向正反应进行,此时v(正)>v(逆),
,故平衡向正反应进行,此时v(正)>v(逆),
故答案为:否;大于。