题目内容
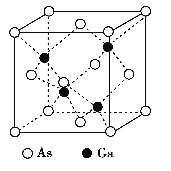
【题目】锌锰干电池是最早的实用电池。现用下列工艺回收正极材料中的金属(部分条件未给出)。

(1)碱性锌锰电池反应为:Zn+2MnO2+2H2O=Zn(OH)2+2MnO(OH),电解质是KOH, MnO(OH)中Mn的化合价为:_____,正极反应式为:__________。
(2)黑粉的主要成份为 MnO2和石墨,写出反应①的化学方程式:________
(3)MnO2的转化率与温度的关系如下表:
温度/℃ | 20 | 40 | 60 | 80 | 100 |
转化率/℃ | 86.0 | 90.0 | 91.3 | 92.0 | 92.1 |
生产中常选反应温度为80℃,其理由是:___________。
(4)“沉锰”过程中生成碱式碳酸锰[MnCO36Mn(OH)25H2O],写出其离子反应方程式:_______。滤液③中可回收的物质为:________(填化学式)。
(5)用硫酸酸化的![]() 浆液可吸收工业废气中的
浆液可吸收工业废气中的![]() 生成
生成![]() ,已知浆液中
,已知浆液中![]() 含量为
含量为![]() ,工业废气中
,工业废气中![]() 含量为
含量为![]() ,
, ![]() 的吸收率可达90%,则处理1000
的吸收率可达90%,则处理1000![]() 工业尾气,可得到
工业尾气,可得到![]() 的质量为____kg(用含字母的代数式表示)。
的质量为____kg(用含字母的代数式表示)。
【答案】+3价 MnO2+H2O+e-=MnO(OH)+OH- MnO2+2FeSO4+2H2SO4=MnSO4+Fe2(SO4)3+2H2O 由表格中的数据可知,MnO2的转化率随温度的升高而升高,80℃时MnO2的转化率已经较高,更高的温度会增加能耗,增大生产成本,得不偿失 Mn2++7CO32-+11H2O=MnCO3·6Mn(OH)2·5H2O↓+6CO2↑ Na2SO4 ![]() 或
或![]()
【解析】
废旧锌锰干电池经过预处理得到黑粉,黑粉主要成分为二氧化锰与石墨,则反应①是MnO2、FeSO4和H2SO4发生的氧化还原反应生成硫酸铁与硫酸锰,并将不溶物二氧化锰与石墨过滤,得到的滤液经碳酸钠调节pH=4.5,使铁离子转化为氢氧化铁沉淀而除去,得到的滤液主要成分为硫酸锰, “沉锰”过程中碳酸根离子与溶液中锰离子反应,得到碱式碳酸锰沉淀[MnCO36Mn(OH)25H2O]沉淀与硫酸钠,过滤后所得的滤液③溶质为硫酸钠,滤渣③再经硫酸酸化得到硫酸锰溶液,最终蒸发浓缩,过滤干燥得到MnSO4H2O,据此分析作答。
(1)碱性锌锰电池反应为:Zn+2MnO2+2H2O=Zn(OH)2+2MnO(OH),电解质是KOH,活泼金属Zn为该电池的负极材料,MnO(OH)中氧为-2价,氢为+1价,则Mn的化合价为:+3价;正极MnO2得到电子产生MnO(OH),电极反应式为:MnO2+H2O+e-=MnO(OH)+OH-;
(2)黑粉的主要成份为 MnO2和石墨,其反应的化学方程式为:MnO2+2FeSO4+2H2SO4=MnSO4+Fe2(SO4)3+2H2O;
(3)由表格中的数据可知,MnO2的转化率随温度的升高而升高,80℃时MnO2的转化率已经较高,更高的温度会增加能耗,增大生产成本,得不偿失,故生产中常选反应温度为80℃,故答案为:由表格中的数据可知,MnO2 的转化率随温度的升高而升高,80℃时MnO2的转化率已经较高,更高的温度会增加能耗,增大生产成本,得不偿失;
(6)“沉锰”过程中碳酸钠与硫酸锰反应生成碱式碳酸锰![]() ,碳酸钠水解生成氢氧化钠、生成氢氧化锰沉淀后促进水解放出二氧化碳,反应的离子方程式为
,碳酸钠水解生成氢氧化钠、生成氢氧化锰沉淀后促进水解放出二氧化碳,反应的离子方程式为![]() ,根据该反应方程式可知,滤液③中可回收的物质为:Na2SO4,故答案为:
,根据该反应方程式可知,滤液③中可回收的物质为:Na2SO4,故答案为: ![]() ;Na2SO4;
;Na2SO4;
(7)用硫酸酸化的MnO2浆液可吸收工业废气中的SO2生成MnSO4·H2O,反应的方程式为MnO2+SO2+H2O=MnSO4·H2O。1000![]() 工业尾气中含有的SO2的物质的量为
工业尾气中含有的SO2的物质的量为![]() =
=![]() mol,则生成的MnSO4·H2O的物质的量为
mol,则生成的MnSO4·H2O的物质的量为![]() mol×90%=
mol×90%=![]() mol,质量为
mol,质量为![]() mol×169g/mol=
mol×169g/mol=![]() g=
g= ![]() 或
或![]() kg。
kg。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】草酸是一种常用的还原剂,某校高三化学小组探究草酸被氧化的速率问题。
实验Ⅰ | 试剂 | 混合后 溶液pH | 现象 (1h后溶液) | ||
试管 | 滴管 | ||||
| a | 4mL0.01mol·L1 KMnO4溶液,几滴浓H2SO4 | 2mL0.3mol·L1H2C2O4 溶液 | 2 | 褪为无色 |
b | 4mL0.01mol·L1KMnO4溶液,几滴浓NaOH | 7 | 无明显变化 | ||
c | 4mL0.01mol·L1 K2Cr2O7溶液,几滴浓H2SO4 | 2 | 无明显变化 | ||
d | 4mL0.01mol·L1 K2Cr2O7溶液,几滴浓NaOH | 7 | 无明显变化 | ||
(1)H2C2O4是二元弱酸,写出H2C2O4溶于水的电离方程式:_____________。
(2)实验I试管a中KMnO4最终被还原为Mn2+,该反应的离子方程式为:________。
(3)瑛瑛和超超查阅资料,实验I试管c中H2C2O4与K2Cr2O7溶液反应需数月时间才能完成,但加入MnO2可促进H2C2O4与K2Cr2O7的反应。依据此资料,吉吉和昊昊设计如下实验证实了这一点。
实验III | 实验IV | ||
实验操作 |
|
|
|
实验现象 | 6 min后固体完全溶解,溶液橙色变浅,温度不变 | 6 min后固体未溶解,溶液颜色无明显变化 | 6 min后固体未溶解,溶液颜色无明显变化 |
实验IV的目的是:_______________________。
(4)睿睿和萌萌对实验II继续进行探究,发现溶液中Cr2O72- 浓度变化如图:

臧臧和蔡蔡认为此变化是通过两个过程实现的。
过程i.MnO2与H2C2O4反应生成了Mn2+。
过程ii.__________________________________。
①查阅资料:溶液中Mn2+能被PbO2氧化为MnO4-。针对过程i,可采用如下方法证实:将0.0001molMnO2加入到6mL____________中,固体完全溶解;从中取出少量溶液,加入过量PbO2固体,充分反应后静置,观察到_______________。
②波波和姝姝设计实验方案证实了过程ii成立,她们的实验方案是________。
(5)综合以上实验可知,草酸发生氧化反应的速率与__________________有关。
【题目】某小组同学探究物质的溶解度大小与沉淀转化方向之间的关系。已知:

(1)探究BaCO3和BaSO4之间的转化,实验操作:
试剂A | 试剂B | 试剂C | 加入盐酸后的现象 | |
实验Ⅰ | BaCl2 | Na2CO3 | Na2SO4 | …… |
实验Ⅱ | Na2SO4 | Na2CO3 | 有少量气泡产生,沉淀部分溶解 |
①实验Ⅰ说明BaCO3全部转化为BaSO4,依据的现象是加入盐酸后,__________
②实验Ⅱ中加入稀盐酸后发生反应的离子方程式是_______。
③实验Ⅱ说明沉淀发生了部分转化,结合BaSO4的沉淀溶解平衡解释原因:______
(2)探究AgCl和AgI之间的转化,实验Ⅲ:
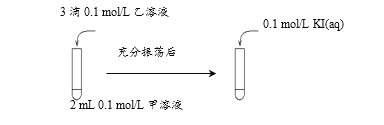
实验Ⅳ:在试管中进行溶液间反应时,同学们无法观察到AgI转化为AgCl,于是又设计了如下实验(电压表读数:a>c>b>0)。

注:其他条件不变时,参与原电池反应的氧化剂(或还原剂)的氧化性(或还原性)越强,原电池的电压越大;离子的氧化性(或还原性)强弱与其浓度有关。
① 实验Ⅲ证明了AgCl转化为AgI,甲溶液可以是______(填序号)。
a. AgNO3溶液 b. NaCl溶液 c. KI溶液
② 实验Ⅳ的步骤ⅰ中,B中石墨上的电极反应式是 _______________
③ 结合信息,解释实验Ⅳ中b<a的原因:______。
④ 实验Ⅳ的现象能说明AgI转化为AgCl,理由是_______