题目内容
一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为CH3CH2OH-4e-+H2O=CH3COOH+4H+。下列有关说法正确的是
| A.正极上发生的反应是:O2+4e-+2H2O=4OH- |
| B.该电池反应的化学方程式为:CH3CH2OH+3O2点燃2CO2+3H2O |
| C.检测时,电解质溶液中的H+向正极移动 |
| D.若有0.4mol电子转移,则在标准状况下消耗4.48L氧气 |
C
解析试题分析: A.由负极可知电解池溶液呈酸性,则燃料电池中,氧气在正极得电子被还原生成水,正极反应式为O2+4e-+4H+=2H2O,故A错误;B.酸性乙醇燃料电池的负极反应为CH3CH2OH-4e-+H2O=CH3COOH+4H+,可知乙醇被氧化生成乙酸和水,总反应式为CH3CH2OH+O2=CH3COOH+H2O,但反应条件下不是燃烧,故B错误;C.原电池中,阳离子向正极移动,故C正确;D.氧气得电子被还原,化合价由0价降低到-2价,若有0.4mol电子转移,则应有0.1mol氧气被还原,在标准状况下的体积为2.24L,故D错误;故选C。
考点:考查原电池的工作原理。

美国海军海底战事中心与麻省理工大学共同研制成功了用于潜航器的镁—过氧化氢燃料电池系统。其工作原理如图所示。以下说法中错误的是 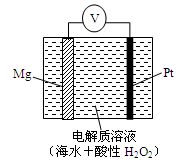
| A.电池的负极反应为:Mg – 2e-= Mg2+ |
| B.电池的正极产生的还原产物是水 |
| C.电池工作时,H+向负极移动 |
| D.电池工作一段时间后,溶液的pH增大 |
氢氧燃料电池是一种高效、环境友好的发电装置,它是以铂作电极,KOH溶液作电解液,总反应为:2H2 + O2 = 2H2O,正极反应为:O2 + 2H2O + 4e- = 4OH-下列叙述不正确的是( )
| A.H2通入负极区 | B.O2通入正极区 |
| C.负极发生氧化反应 | D.正极发生氧化反应 |
铁棒和石墨棒用导线连接后,浸入0. 01mol/L 的氯化钠溶液中,下列说法正确的是
| A.铁棒附近产生OH— | B.铁棒质量减少 |
| C.石墨棒上放出氢气 | D.石墨棒上放出氧气 |
用石墨电极电解100 mL H2SO4与CuSO4的混合溶液,通电一段时间后,两极均收集到2.24 L气体(标准状况),则原混合溶液中Cu2+的物质的量浓度为( )
| A.1 mol·L-1 | B.2 mol·L-1 | C.3 mol·L-1 | D.4 mol·L-1 |
下图是在航天用高压氢镍电池基础上发展起来的一种金属氢化物镍电池(MH-Ni电池)。下列有关说法不正确的是
| A.放电时正极反应为:NiOOH+H2O+e-→Ni(OH)2+OH- |
| B.电池的电解液可为KOH溶液 |
| C.充电时负极反应为:MH+OH-→+H2O+M+e- |
| D.MH是一类储氢材料,其氢密度越大,电池的能量密度越高 |
铝电池性能优越,Al—Ag2O电池可用作水下动力电源,其原理如图所示。下列说法正确的是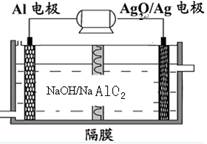
| A.电池负极反应式2Ag+2OH--2e-=" Ag" 2O+H2O |
| B.放电时电池负极附近PH减小 |
| C.电池总反应式2Al+3Ag2O+6H+ =2Al3++6Ag+3H2O |
| D.电解液中Na+通过隔膜由右向左移动 |
将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( )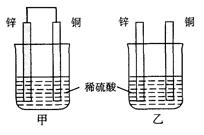
| A.两烧杯中铜片表面均无气泡产生 | B.甲中铜片是正极,乙中铜片是负极 |
| C.两烧杯中溶液的pH均增大 | D.产生气泡的速度甲比乙慢 |
500 mL KNO3和Cu(NO3)2的混合溶液中c(NO3-)=6.0 mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4 L气体(标准状况),假定电解后溶液体积仍为500 mL,下列说法正确的是( )
| A.原混合溶液中c(K+)为1 mol·L-1 | B.上述电解过程中共转移4 mol电子 |
| C.电解得到的Cu的物质的量为0.5 mol | D.电解后溶液中c(H+)为2 mol·L-1 |