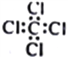题目内容
【题目】下表是元素周期表的一部分,根据A~H在元素周期表中的位置,用元素符号或化学式回答下列问题:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
1 | A | |||||||
2 | D | E | G | |||||
3 | B | C | F | H |
(1)上表中,元素金属性最强的是________(填元素符号)。
(2)写出D的原子结构示意图:__________
(3)B与C的原子半径比较: ________C (填“>”或“<”)。G与H的非金属性比较:G ________ H(填“>”或“<”)。
(4)A与H形成化合物的电子式:_______
(5)写出B的最高价氧化物对应水化物与H的气态氢化物的水溶液反应的离子方程式:______。
【答案】Na ![]() > >
> > ![]() H++OH
H++OH![]() =H2O
=H2O
【解析】
根据元素周期表,A为H,D为C,E为N,G为F,B为Na,C为Al,F为P,H为Cl,据此分析;
(1)根据同周期从左向右金属性减弱,同主族从上到下金属性增强,推出该表格中金属性最强元素是B,即为Na;
(2)D位于第二周期IVA族,即D为C,其原子结构示意图为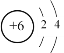 ;
;
(3)同周期从左向右原子半径减小,即Na的半径大于Al;同主族从上到下非金属性减弱,即F的非金属性强于Cl;
(4)A为H,H为Cl,化合物是HCl,其电子式为![]() ;
;
(5)B的最高价氧化对应的水化物为NaOH,H的最高价氧化物对应水化物是HClO4,两者都是强电解质,反应的离子方程式为H++OH-=H2O。

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案
相关题目