题目内容
【题目】在元素周期表中,最容易找到半导体材料的合理位置是
A.周期表的右上角B.过渡元素区
C.金属元素和非金属元素交界处D.周期表的左下角
【答案】C
【解析】
在金属元素与非金属元素的分界线附近的元素,通常既具有金属性又具有非金属性,可以找到半导体材料。
A.周期表右上角的元素常用于制备农药,故A错误;
B.过渡元素常用于制备催化剂材料,故B错误;
C.在金属元素和非金属元素交接区域的元素通常既具有金属性又具有非金属性,可以用来做良好的半导体材料,如硅等,故C正确;
D.周期表左下角的元素具有较强的金属性,为电的良导体,不可以作半导体材料,故D错误;
答案选C。

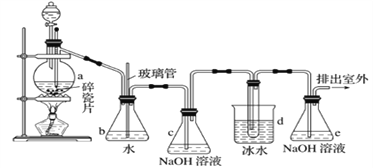
【题目】1,2-二溴乙烷可作抗爆剂的添加剂。如图为实验室制备1,2-二溴乙烷的装罝图, 图中分液漏斗和烧瓶a中分别装有浓H2SO4和无水乙醇,d装罝试管中装有液溴。
已知:Ⅰ.CH3CH2OH![]() CH2=CH2↑+H2O;2CH3CH2OH
CH2=CH2↑+H2O;2CH3CH2OH![]() CH3CH2OCH2CH3(乙醚)+H2O
CH3CH2OCH2CH3(乙醚)+H2O
Ⅱ.相关数据列表如下:
乙醇 | 1,2-二溴乙烷 | 乙醚 | 溴 | |
状态 | 无色液体 | 无色液体 | 无色液体 | 红棕色液体 |
密度/g·cm-3 | 0.79 | 2.18 | 0.71 | 3.10 |
沸点/℃ | 78.5 | 131.4 | 34.6 | 58.8 |
熔点/℃ | -114.3 | 9.79 | - 116.2 | -7.2 |
水溶性 | 混溶 | 难溶 | 微溶 | 可溶 |
(1)已知条件Ⅰ中有两个反应,其中第二个反应所属反应类型为____________________。
(2)实验中应迅速将温度升高到170℃左右的原因是______________________________。
(3)安全瓶b在实验中有多重作用。其一可以检查实验进行中d装罝中导管是否发生堵塞,请写出发生堵塞时瓶b中的现象:_______________________________;如果实验时d装罝中导管堵塞,你认为可能的原因是_______________________________________________;安全瓶b还可以起到的作用是__________________
(4)容器c、e中都盛有NaOH溶液,c中NaOH溶液的作用是________________________________。
(5)除去产物中少量未反应的Br2后,还含有的主要杂质为___________,要进一步提纯,下列操作中必需的是_____________ (填字母)。
A.重结晶 B.过滤 C.蒸馏 D.萃取
(6)实验中也可以撤去d装罝中盛冰水的烧杯,改为将冷水直接加入到d装罝的试管中,则此时冷水除了能起到冷却1,2-二溴乙烷的作用外,还可以起到的作用是____________________________。