题目内容
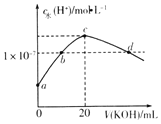
【题目】在25mL0.1molL—1NaOH溶液中逐滴加入0.1molL-1 CH3COOH溶液,曲线如图所示,有关粒子浓度关系正确的是( )
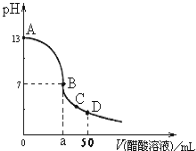
A.在A、B间任一点,溶液中一定都有c(Na+)+c(H+)=c(CH3COO-)+(OH-)
B.在B点,a>25,且有c(Na+)=c(CH3COO-)=c(OH-)=c(H+)
C.在C点:c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
D.在D点:c(CH3COO-)+c(CH3COOH)=c(Na+)
【答案】A
【解析】
试题A、根据电荷守恒知溶液中一定都有c(Na+)+c(H+)=c(CH3COO-)+(OH-),正确;B、NaOH溶液中加入CH3COOH溶液,当二者物质的量相等时恰好生成CH3COONa,CH3COO-水解,溶液呈碱性,但此时溶液为中性,故只有醋酸过量,即a>25,根据电荷守恒知c(Na+)+c(H+)=c(CH3COO-)+(OH-),又此时溶液为中性,因此c(OH-)=c(H+),c(Na+)=c(CH3COO-) ,但c(H+)远小于c(Na+),错误;C、C点溶液为醋酸钠和醋酸的混合溶液,溶液呈酸性,c(CH3COO-)>c(Na+)>c(H+)>c(OH-),错误;D、根据物料守恒知在D点:c(CH3COO-)+c(CH3COOH)=2c(Na+),错误。

 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案【题目】磷和砷的相关化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:
(1)红磷是巨型共价分子,无定型结构,下列方法能证明红磷是非晶体的是_____。
A 质谱法 B 原子发射光谱法 C 核磁共振谱法 D X射线行射法
(2)第一电离能介于Al、P之间的第三周期元素有___种。GaCl3分子中心原子的杂化方式为___。
(3)基态As原子的核外电子排布式为_____,As原子的逐级电离能数据如下:
第一电离能 | 第二电离能 | 第三电离能 | 第四电离能 | 第五电离能 | 第六电离能 |
947.0 | 1798 | 2735 | 4837 | 6043 | 12310 |
为什么第五电离能与第六电离能相差较大_____________。
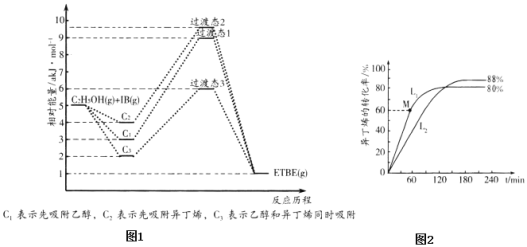
(4)如图所示,每条折线表示周期表ⅣA-ⅦA中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是___________。

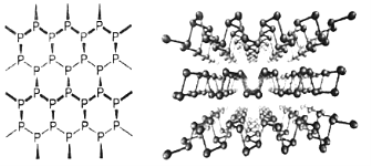
(5)黑磷是新型二维半导体材料,具有片层结构(如下图所示),P原子的杂化形式为_____,层与层之间的相互作用为_____。
(6)GaAs的熔点为1238℃,且熔融状态不导电,其晶胞结构如下图所示,该晶体的类型为_____,每个As原子周围最近的As原子数目为_____,一个GaAs晶胞中配位键的数目为_____。
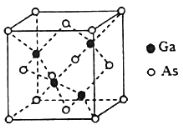
(7)已知GaAs的密度为dg/cm3,摩尔质量为Mg/mol,阿伏加德罗常数用NA表示,则晶胞中最近的As和Ga原子核间距为_____ nm(列式表示)。