题目内容
【题目】轿车进入家庭,给人们带来了极大方便,但排出的尾气给环境带来了污染。现在已经研制出了汽车尾气处理装置并已投入使用,它可将汽车尾气中的有害成分转化为对环境无害的物质。某研究小组利用如图装置模拟汽车尾气的处理过程,请回答下列问题:
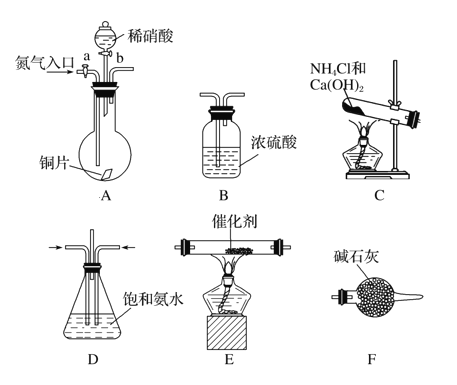
(1)仪器的连接顺序如下,请把装置代号填入下列括号中:_______
![]()
(2)C中的化学反应方程式为___________________________________________________________________。
(3)E中的化学反应方程式为________________________________________________。
(4)D装置的作用是
①_____________________________________,
②通过观察气泡数目调节气体流速。
(5)有同学认为,按上述方案两种气体的体积比例不易得到很好的控制,提出改变装置连接顺序为
![]()
但D中的液体需改成________。即便如此,该实验还存在明显缺陷,你认为它是
_______________________________________________________。
(6)科学研究的最终目的是应用于生产与生活实际,造福人类。你认为汽车尾气处理研究的方向是________(填字母)。
A.选择适宜的氧化剂,适宜的温度,高效催化剂
B.选择适宜的还原剂,适宜的温度,高效催化剂
C.选择适宜的还原剂,高温,高效催化剂
【答案】 F 2NH4Cl+Ca(OH)2![]() 2NH3↑+CaCl2+2H2O 6NO+4NH3
2NH3↑+CaCl2+2H2O 6NO+4NH3![]() 5N2+6H2O NO与NH3充分混合 CCl4(或难挥发有机溶剂) 缺少尾气处理装置 B
5N2+6H2O NO与NH3充分混合 CCl4(或难挥发有机溶剂) 缺少尾气处理装置 B
【解析】本题考查实验方案设计与评价,(1)A装置制备NO,C装置制备的是NH3,NH3与NO生成无毒的物质,即N2和H2O,反应方程式为6NO+4NH3![]() 5N2+6H2O,此反应在E中进行,因此D和E装置之间的装置为干燥装置,即为F;(2)C是制备氨气的装置,反应方程式为::2NH4Cl+Ca(OH)2
5N2+6H2O,此反应在E中进行,因此D和E装置之间的装置为干燥装置,即为F;(2)C是制备氨气的装置,反应方程式为::2NH4Cl+Ca(OH)2 ![]() CaCl2+2NH3↑+2H2O;(3)根据(1)的分析,反应方程式为:6NO+4NH3
CaCl2+2NH3↑+2H2O;(3)根据(1)的分析,反应方程式为:6NO+4NH3![]() 5N2+6H2O;(4)D装置的作用是①使氨气和NO充分混合,②通过观察气泡数目调节气体的流速,达到原料的最大利用;(5)氨气极易溶于水,因此D装置不能盛放含水的液体,因此盛放四氯化碳或难挥发性的有机物,氨气与NO有毒,应防止污染环境,因此缺少尾气处理装置;(6)汽车尾气,根据反应,NO转化成N2,NO中N的化合价降低,因此应选择适宜的还原剂,适宜的温度和催化剂,故B正确。
5N2+6H2O;(4)D装置的作用是①使氨气和NO充分混合,②通过观察气泡数目调节气体的流速,达到原料的最大利用;(5)氨气极易溶于水,因此D装置不能盛放含水的液体,因此盛放四氯化碳或难挥发性的有机物,氨气与NO有毒,应防止污染环境,因此缺少尾气处理装置;(6)汽车尾气,根据反应,NO转化成N2,NO中N的化合价降低,因此应选择适宜的还原剂,适宜的温度和催化剂,故B正确。

【题目】【福建省福州第一中学2017届高三下学期模考4】利用如图所示装置进行下列实验,实验现象与结论均正确的是( )

选项 | 实验试剂 | 实验现象 | 实验结论 | ||
a | b | c | |||
A | 浓氨水 | 碱石灰 | FeCl2溶液 | 产生白色沉淀,迅速变为灰绿色,最后变为红褐色 | 氨气具有氧化性 |
B | 稀硫酸 | FeS | AgCl悬浊液 | 悬浊液由白色变为黑色 | Ksp(AgCl)>Ksp(Ag2S) |
C | 浓硝酸 | 铜 | BaSO3悬浊液 | 悬浊液变澄清 | +4价硫具有还原性 |
D | 浓盐酸 | KMnO4 | 紫色石蕊试液 | 溶液先变红后褪色 | Cl2有酸性和漂白性 |
【题目】增强铝的耐腐蚀性,现以铅蓄电池以外电源,以Al作阳极、Pb作阴极,电解稀硫酸,使表面表面的氧化膜增厚。反应原理如下:电池:Pb(s)+PbO2(s)+2H2SO4(aq)═2PbSO4(s)+2H2O(I)
电解池:2Al+3H2O![]() Al2O3+3H2↑
Al2O3+3H2↑
电解过程中,以下判断正确的是
电池 | 电解池 | |
A | H+移向Pb电极 | H+移向Pb电极 |
B | 每消耗3molPb | 生成2molAl2O3 |
C | 正极:PbO2+4H++2e-═Pb2++2H2O | 阳极:2Al+3H2O-6e-═Al2O3+6H+ |
D |
|
|
A. A B. B C. C D. D








