题目内容
【题目】已知反应H2(g)+![]() O2(g)===H2O(g)的能量变化如图所示,a、b、c表示能量变化,为正值,单位为kJ,下列说法正确的是( )
O2(g)===H2O(g)的能量变化如图所示,a、b、c表示能量变化,为正值,单位为kJ,下列说法正确的是( )

A. H2(g)+![]() O2(g)===H2O(g) ΔH=c kJ·mol-1
O2(g)===H2O(g) ΔH=c kJ·mol-1
B. 2H2O(g)===2H2(g)+O2(g) ΔH=-2(a-b)kJ·mol-1
C. 1 mol氢气与0.5 mol氧气总能量为a kJ
D. 2 mol氢气与1 mol氧气完全反应生成2 mol液态水放出的热量小于2(b-a) kJ
【答案】B
【解析】A. 根据图像,H2(g)+![]() O2(g)===H2O(g)的反应放热,ΔH=-c kJ·mol-1,故A错误;B.根据A的分析, 2H2O(g)===2H2(g)+O2(g)反应吸热,ΔH=2c kJ·mol-1=-2(a-b)kJ·mol-1,故B正确;C. 根据图像,断开1 mol氢气与0.5 mol氧气中的化学键,需要吸收a kJ能量,1 mol氢气与0.5 mol氧气总能量大于a kJ,故C错误;D. 水蒸气转化为液态水会放出热量,因此2 mol氢气与1 mol氧气完全反应生成2 mol液态水放出的热量大于2(b-a) kJ,故D错误;故选B。
O2(g)===H2O(g)的反应放热,ΔH=-c kJ·mol-1,故A错误;B.根据A的分析, 2H2O(g)===2H2(g)+O2(g)反应吸热,ΔH=2c kJ·mol-1=-2(a-b)kJ·mol-1,故B正确;C. 根据图像,断开1 mol氢气与0.5 mol氧气中的化学键,需要吸收a kJ能量,1 mol氢气与0.5 mol氧气总能量大于a kJ,故C错误;D. 水蒸气转化为液态水会放出热量,因此2 mol氢气与1 mol氧气完全反应生成2 mol液态水放出的热量大于2(b-a) kJ,故D错误;故选B。

练习册系列答案
相关题目
【题目】下列图中的实验方案,能达到实验目的的是( )
A | B | C | D | |
实验方案 |
|
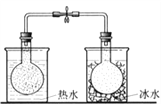
将NO2球浸泡在冰水和热水中 |
|
|
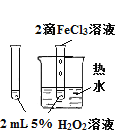
实验 目的 | 验证FeCl3对H2O2 分解反应有催化作用 | 探究温度对平衡 2NO2 | 除去CO2气体中混有的SO2 | 比较HCl、H2CO3和H2SiO3的酸性强弱 |
A. A B. B C. C D. D