题目内容
5.下列说法正确的是( )| A. | 向磁性氧化铁溶解于足量稀盐酸后的溶液中滴加酸性KMnO4溶液,紫红色消失,表明溶液中含有Fe2+ | |
| B. | 用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定是钠盐溶液 | |
| C. | FeCl3、FeCl2、Fe(OH)3三种化合物都可以通过化合反应制得 | |
| D. | 向NaAlO2溶液中滴加NaHCO3溶液,有沉淀和气体生成 |
分析 A.盐酸中氯离子具有还原性,能够还原高锰酸钾;
B.焰色反应为元素的性质;
C.依据物质的性质结合化合反应定义解答;
D.NaHCO3溶液与NaAlO2溶液混合产生白色沉淀氢氧化铝;
解答 解:A.向磁性氧化铁溶解于足量稀盐酸后的溶液中滴加酸性KMnO4溶液,紫红色消失,不能表明溶液中含有Fe2+,因为盐酸中的氯离子具有还原性,能够还原高锰酸钾,使高锰酸钾褪色,故A错误;
B.焰色反应为元素的性质,此溶液也可能是NaOH,NaOH为碱,不是盐,故B错误;
C.氯化亚铁与氯气反应生成氯化铁,氯化铁与铁反应生成氯化亚铁,氢氧化铁、氧气和水反应生成氢氧化铁,都属于化合反应,故C正确;
D.NaHCO3溶液与NaAlO2溶液混合产生白色沉淀氢氧化铝,无气体放出,所以不符合题意,故D错误;
故选:C.
点评 本题考查了元素化合物知识,熟悉二价铁离子、氯离子的还原性,熟悉焰色反应是元素性质是解题关键,题目难度不大,侧重考查学生对基础知识掌握熟练程度.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.下列变化:①液态水汽化②将胆矾加热变为白色粉末 ③浓硫酸稀释 ④氯酸钾分解⑤生石灰跟水反应;属于吸热反应的是( )
| A. | ②④ | B. | ①④ | C. | ②③ | D. | ①④⑤ |
16.在对应的温度下,体积均为2L的三个恒容密闭容器中发生如下可逆反应:N2O4(g)?2NO2(g)△H=+57kJ/mol,实验测得有关数据如下表:
下列叙述正确的是( )
| 容器编号 | 温度 | 起始时各物质的物质的量/mol | 达到平衡时体系能量的变化 | 达到平衡所需时间 | |
| N2O4 | NO2 | ||||
| ① | T1 | 2 | 0 | 吸热22.8kJ | 2min |
| ② | T2 | 0 | 4 | 放热Q(Q>0)kJ | … |
| ③ | T3 | 3 | 1 | … | … |
| A. | 容器①中,从起始到平衡时,用NO2表示的平均反应速率v(NO2)为0.2mol(L•min) | |
| B. | 若容器①在恒温恒压下达平衡,该条件下的平衡常数等于0.2 | |
| C. | 若Q<34.2kJ,则T1>T2 | |
| D. | 容器③在达平衡前,v(正)<v(逆) |
13.白磷在高压下隔绝空气加热后急速冷却,可得钢灰色固体--黑磷,其转化过程如下:白磷$\stackrel{12159MPa,473K,隔绝空气}{→}$黑磷,黑磷性质稳定,结构与石墨相似.下列叙述正确的是( )
| A. | 黑磷与白磷互为同分异构体 | B. | 黑磷能导电 | ||
| C. | 白磷转化为黑磷是物理变化 | D. | 黑磷能在空气中自燃 |
20.一块金属钠置于空气中,最终得到的产物是( )
| A. | Na2O | B. | NaOH | C. | Na2O2 | D. | Na2CO3 |
10. 25℃时,部分物质的电离平衡常数如表所示:
25℃时,部分物质的电离平衡常数如表所示:
请回答下列问题:
(1)CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为CH3COOH>H2CO3>HClO.
(2)同浓度的CH3COO-、HCO3-、CO32-、ClO-结合H+的能力由强到弱的顺序为CO32->ClO->HCO3->CH3COO-.
(3)常温下0.1mol•L-1的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是A.
A.c(H+) B.$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ C.c(H+)•c(OH-) D.$\frac{c(O{H}^{-})}{c({H}^{+})}$E.$\frac{cC{H}_{3}CO{O}^{-}•c{H}^{+}}{cC{H}_{3}COOH}$
若该溶液升高温度,上述5种表达式的数据增大的是ABCE.
(4)体积为10mL pH=2的醋酸溶液与一元酸HX分别加水稀释至1 000mL,稀释过程中pH变化如图所示,则相同条件下HX的电离平衡常数大于(填“大于”、“等于”或“小于”)醋酸的电离平衡常数;理由是稀释相同倍数,HX的pH变化比CH3COOH的大,酸性强,电离平衡常数大,稀释后,HX溶液中由水电离出来的c(H+)大于(填“大于”、“等于”或“小于”)醋酸溶液中由水电离出来的c(H+),理由是HX酸性强于CH3COOH的,稀释后HX溶液中的c(H+)小于CH3COOH溶液中的c(H+),所以其对水电离的抑制能力也较弱.
 25℃时,部分物质的电离平衡常数如表所示:
25℃时,部分物质的电离平衡常数如表所示:| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
(1)CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为CH3COOH>H2CO3>HClO.
(2)同浓度的CH3COO-、HCO3-、CO32-、ClO-结合H+的能力由强到弱的顺序为CO32->ClO->HCO3->CH3COO-.
(3)常温下0.1mol•L-1的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是A.
A.c(H+) B.$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ C.c(H+)•c(OH-) D.$\frac{c(O{H}^{-})}{c({H}^{+})}$E.$\frac{cC{H}_{3}CO{O}^{-}•c{H}^{+}}{cC{H}_{3}COOH}$
若该溶液升高温度,上述5种表达式的数据增大的是ABCE.
(4)体积为10mL pH=2的醋酸溶液与一元酸HX分别加水稀释至1 000mL,稀释过程中pH变化如图所示,则相同条件下HX的电离平衡常数大于(填“大于”、“等于”或“小于”)醋酸的电离平衡常数;理由是稀释相同倍数,HX的pH变化比CH3COOH的大,酸性强,电离平衡常数大,稀释后,HX溶液中由水电离出来的c(H+)大于(填“大于”、“等于”或“小于”)醋酸溶液中由水电离出来的c(H+),理由是HX酸性强于CH3COOH的,稀释后HX溶液中的c(H+)小于CH3COOH溶液中的c(H+),所以其对水电离的抑制能力也较弱.
17.如图有关实验操作正确的是( )
| A. | 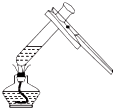 加热液体 | B. | 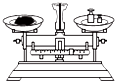 称取10.05g氢氧化钠 | ||
| C. | 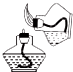 点燃酒精灯 | D. |  量取8.5mL液体 |
14.要从硝酸钾和食盐(少量)的混合物中,分离出较纯净的硝酸钾,应把它们( )
| A. | 溶解、过滤 | B. | 制成饱和溶液,降温后再过滤 | ||
| C. | 加热、冷却后结晶 | D. | 溶解、过滤后结晶 |
15.下列解释实验现象的反应方程式正确的是( )
| A. | 切开的金属Na暴露在空气中,光亮表面逐渐变暗:2Na+O2═Na2O2 | |
| B. | 电解饱和食盐水:2NaCl$\frac{\underline{\;电解\;}}{\;}$2Na+Cl2↑ | |
| C. | Na2O2在潮湿空气中放置一段时间,变成白色黏稠物:2Na2O2+2CO2═2Na2CO3+O2 | |
| D. | 向NaHCO3溶液中加入少量的澄清石灰水,出现白色沉淀:2HCO${\;}_{3}^{-}$+Ca2++2OH-═CaCO3↓+CO32-+2H2O |