题目内容
【题目】为确认HCl、H2CO3和H2SiO3的酸性强弱,某学生设计了如图所示的装置,一次实验即可达到目的(不必选其他酸性物质)。请据此完成下列问题:
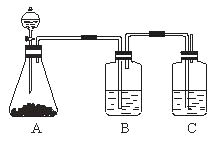
(1)锥形瓶中装某可溶性正盐溶液,分液漏斗所盛试剂应为______。
(2)装置B所盛试剂是______,其作用是___________。
(3)装置C所盛试剂是______,C中反应的离子方程式是___________。
【答案】 盐酸 饱和NaHCO3溶液 除去盐酸中挥发出的HCl气体 Na2SiO3溶液 CO2+SiO32-+H2O=CO32-+H2SiO3↓
【解析】
根据较强酸制取较弱酸可知,较强酸能和较弱酸盐反应生成较弱酸,较弱酸能制取更弱的酸,要想验证HCl、H2CO3、H2SiO3的酸性强弱,用盐酸和碳酸盐反应制取二氧化碳,用二氧化碳和硅酸钠溶液制取硅酸,根据实验现象确定酸的相对强弱。
(1)用盐酸和碳酸盐反应制取二氧化碳,用二氧化碳和硅酸钠溶液制取硅酸,因此锥形瓶中加入碳酸钠溶液,分液漏斗中的试剂为盐酸;
(2)盐酸有挥发性,导致二氧化碳气体中含有HCl,会对实验造成干扰,所以B装置要盛放能除去HCl,且不能产生新的杂质、不能和二氧化碳反应的药品,一般常用饱和碳酸氢钠溶液,作用是除去二氧化碳中混有的HCl;
(3)根据以上分析可知C为硅酸钠溶液,二氧化碳、水和硅酸钠反应生成碳酸钠和硅酸沉淀,所以看到有沉淀生成,用于验证碳酸的酸性强于硅酸,反应的离子方程式为CO2+SiO32-+H2O=CO32-+H2SiO3↓。

【题目】某校化学研究性学习小组设计实验验证NH3能还原CuO,并对还原产物进行探究。请回答下列问题:
Ⅰ.验证NH3能还原CuO

(1)试剂X为___________________________。
(2)请将提供的装置按合理顺序连接。g→_______________________。
(3)装置B的作用是_______________________。
(4)证明NH3能还原CuO的实验现象是_______________________。
II.探充还原产物的成分
【查阅资料】Cu2O粉末呈红色,在酸性溶液中不稳定:Cu2O+H2SO4(稀)=Cu+CuSO4+H2O。
【实验探究】
实验操作 | 实验现象 | 实验结论 |
取10.4g红色固体于烧杯中,加入足量稀硫酸,充分搅拌,静置 | 若无现象 | ①证明红色固体为_________。 |
若溶液变蓝 | ②证明红色固体肯定含有______,可能含有__________。 | |
取上述反应后的混合物过滤、洗涤、干燥、称重,得固体6.4g | ③经计算,红色固体的成分及其物质的量__________ |


