题目内容
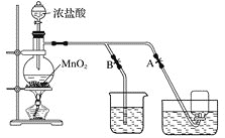
【题目】请用下图所示仪器装罝设计一个电解饱和食盐水,并测定电解产生氢气的 体积和检验氯气氧化性的实验装置。

(1)所选仪器连接时,各接口的顺序是(填各接口的代号字母);a接 , 接 ,b接 , 接 。______________
(2)证明有Cl2生成的实验现象是____________。
(3)实验时,装置中的铁电极接电源的____________极,石墨电极的反应式为____________。
(4)装置E读取气体体积时,应进行的实验操作是____________,若实验结束后装置E的读数(已折算成标准状况)为5.60mL,电解后溶液的体积恰好为50.0mL,则溶液中OH-的浓度为________mol·L-1。
【答案】gfh,dec 装置C中的溶液颜色变蓝 负 2Cl--2e-==Cl2↑ 上下移动装置E,使装置E与D中的液面相平 0.01 mol·L-1
【解析】
用惰性电极电解饱和食盐水时,在阳极上产生氯气,在阴极上产生氢气和氢氧化钠,即a电极为铁,应为电解池的阴极,则生成氢气,可知b端为氯气,A接储气瓶的g→f,把水排入量筒内,用量筒测量出排出的水量,以测定产生H2的体积,用淀粉KI溶液检验氯气,用NaOH溶液吸收氯气,防止污染环境,以此解答该题。
(1)由以上分析可知A接储气瓶的g→f,,把水排入量筒内,用量筒测量出排出的水量,以测定产生H2的体积,B接洗气瓶的d→e,生成的Cl2在洗气瓶中使淀粉碘化钾溶液变蓝,多余的Cl2用NaOH溶液吸收,
故答案为:g;f;h;d;e;c;
(2)氯气可氧化KI,使其变为碘单质,遇淀粉变蓝,则证明有Cl2生成的实验现象为:装置C中的溶液颜色变蓝,
故答案为:装置C中的溶液颜色变蓝;
(3)装置中的铁电极连接电源的负极,所发生的反应为2H++2e═H2↑,石墨电极接电源的正极,所发生的反应为2Cl--2e-==Cl2↑,
故答案为:负;2Cl--2e-==Cl2↑;
(4)为使量气管和水平管内的液面位置保持同一水平,在读取气体体积时,需上下移动装置E,使装置E与D中的液面相平;氢气物质的量为![]() = 0.00025 mol,由2NaCl+2H2O
= 0.00025 mol,由2NaCl+2H2O![]() 2NaOH+Cl2↑+H2↑可知,n(NaOH) = 2 n(H2) = 0.0005 mol,则c(OH) =
2NaOH+Cl2↑+H2↑可知,n(NaOH) = 2 n(H2) = 0.0005 mol,则c(OH) = ![]() = 0.01 molL1,
= 0.01 molL1,
故答案为:上下移动装置E,使装置E与D中的液面相平;0.01 mol·L-1。