题目内容
【题目】Ⅰ.SF6是一种优良的绝缘气体,分子结构中,只存在S—F键,已知1 mol S(s)转化为气态硫原子吸收能量280 kJ,F—F键能为160 kJ·mol-1,S—F键能为330 kJ·mol-1,试写出S(s)和F2(g)反应生成SF6(g)的热化学方程式_______________________________。
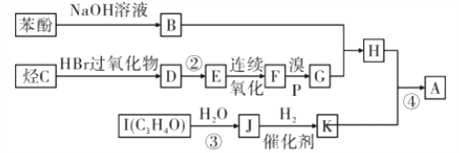
Ⅱ.V、W、X、Y、Z是由四种短周期元素中的2种或3种组成的5种化合物,其中W、X、Z均由2种元素组成,X是导致温室效应的主要气体,Z是天然气的主要成分,Y、W都既能与酸反应,又能与强碱溶液反应。上述5种化合物涉及的四种元素的原子序数之和等于28;V由一种金属元素A和两种非金属元素B与C组成,其化学式构成为A(BC3)3 。它们之间的反应关系如下图:
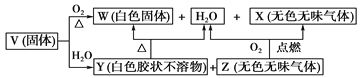
(1)写出物质W的一种用途:__________________________________________________。
(2)写出V与足量NaOH溶液反应的化学方程式:________________________________。
(3)将少量的X通入某种物质的水溶液中可以生成Y,该反应的离子方程式为________________________________________________________________________。
(4)写出气体X的结构式__________。
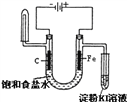
(5)以Z为燃料,活性炭为电极,熔融碳酸盐(如熔融K2CO3)环境下制成燃料电池的负极反应式为_________________________________________________。
【答案】 S(s)+3F2(g)===SF6(g) ΔH=-1 220 kJ·mol-1 作高温耐火材料或冶炼金属铝 Al(CH3)3+NaOH+H2O===NaAlO2+3CH4↑ CO2+2AlO![]() +3H2O===2Al(OH)3↓+CO32─
+3H2O===2Al(OH)3↓+CO32─ ![]() CH4+4CO
CH4+4CO![]() -8e-===5CO2+2H2O
-8e-===5CO2+2H2O
【解析】Ⅰ.反应热△H=反应物总键能-生成物总键能,所以对于S(s)+3F2(g)═SF6(g),其反应热△H=280KJ/mol+3×160KJ/mol-6×330KJ/mol=-1220kJ/mol,热化学方程式为:S(s)+3F2(g)===SF6(g) ΔH=-1 220 kJ·mol-1。
Ⅱ.X是导致温室效应的主要气体,应为CO2,Z是天然气的主要成分,应为CH4,Y、W都既能与酸反应,又能与强碱溶液反应,应为两性化合物,由转化关系可知Y为Al(OH)3,W为Al2O3,则V中含有C、Al、H元素,原子个数比为1:3:9,应为Al(CH3)3。(1)物质W为氧化铝可应用于作高温耐火材料或冶炼金属铝;(2)V[Al(CH3)3]与足量NaOH溶液反应的化学方程式:Al(CH3)3+NaOH+H2O===NaAlO2+3CH4↑。(3)将少量的X(CO2)通入某种物质的水溶液中可以生成Y[Al(OH)3],反应的离子方程式为:CO2+2AlO![]() +3H2O===2Al(OH)3↓+CO32─;(4)写出气体X(CO2)的结构式为
+3H2O===2Al(OH)3↓+CO32─;(4)写出气体X(CO2)的结构式为![]() ;(5) Z(CH4)在活性炭电极上失去电子,与碳酸根离子结合生成二氧化碳,电池的负极反应式为CH4+4CO
;(5) Z(CH4)在活性炭电极上失去电子,与碳酸根离子结合生成二氧化碳,电池的负极反应式为CH4+4CO![]() -8e-===5CO2+2H2O。
-8e-===5CO2+2H2O。