题目内容
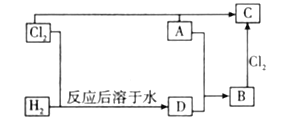
【题目】为探究二元化合物X的组成和性质,某研究小组设计并完成了如下实验(步骤中所加试剂均过量,部分产物已略去)。
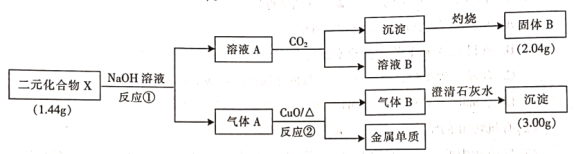
请回答下列问题:
(1)写出X中含有的元素________(用元素符号表示)。
(2)写出反应①的离子方程式___________。
(3)写出反应②的化学方程式___________。
(4)设计实验检验溶液B中所含溶质的阴离子:________。
【答案】Al、C Al4C3+4H2O+4OH-═4AlO2-+3CH4↑ CH4+4CuO![]() 4Cu+CO2+2H2O 取少量溶液B于试管中,加入CaCl2溶液,无明显现象(排除碳酸根离子),再加入NaOH溶液,若生成白色沉淀,则有HCO3-。
4Cu+CO2+2H2O 取少量溶液B于试管中,加入CaCl2溶液,无明显现象(排除碳酸根离子),再加入NaOH溶液,若生成白色沉淀,则有HCO3-。
【解析】
由流程可知,气体A与CuO反应生成气体B可使石灰水变浑浊,气体A为甲烷,沉淀为碳酸钙,其质量为3.0g,由原子守恒可知n(C)=![]() =0.03mol;溶液A与二氧化碳反应生成沉淀为氢氧化铝,灼烧生成B为氧化铝,由Al原子守恒可知n(Al)=
=0.03mol;溶液A与二氧化碳反应生成沉淀为氢氧化铝,灼烧生成B为氧化铝,由Al原子守恒可知n(Al)=![]() ×2=0.04mol,溶液B为碳酸氢钠,以此来解答。
×2=0.04mol,溶液B为碳酸氢钠,以此来解答。
(1)根据分析可知X中含有的元素为Al、C;
(2)根据分析结合题目信息可知反应①中生成了甲烷和偏铝酸钠,所以离子方程式为Al4C3+4H2O+4OH-═4AlO2-+3CH4↑;
(3)反应②的化学方程式为CH4+4CuO![]() 4Cu+CO2+2H2O;
4Cu+CO2+2H2O;
(4)B为碳酸氢钠,检验溶液B中所含溶质的阴离子的方法为取少量溶液B于试管中,加入CaCl2溶液,无明显现象(排除碳酸根离子),再加入NaOH溶液,若生成白色沉淀,则有HCO3-。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目