题目内容
有M、W、X、Y、Z等元素,它们的核电荷数依次增大,且都小于20,其中X、Z是金属元素,其他均为非金属元素,M和Z最外层电子数相同,它们原子的最外层上只有1个电子,W和Y最外层电子数也相同,它们最外层电子数分别是其电子层数的3倍和2倍,X原子最外层电子数等于Y原子最外层电子数的一半,由此可知:
M是________,W是________,X是________,Y是________,Z是________.
答案:H,O,Al,S,K

练习册系列答案
相关题目
 (2013?辽宁一模)[化学--选修3物质结构与性质]
(2013?辽宁一模)[化学--选修3物质结构与性质]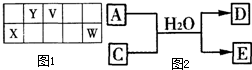 V、W、X、Y、Z是五种常见元素,其中V、W、X、Y四种短周期元素在周期表中的位置如图1示:V、W的最简单气态氢化物M、N混合时有白烟生成,M能使湿润的红色石蕊试纸变蓝.Z是人体血红蛋白中存在的金属元素.请填写下列空白:
V、W、X、Y、Z是五种常见元素,其中V、W、X、Y四种短周期元素在周期表中的位置如图1示:V、W的最简单气态氢化物M、N混合时有白烟生成,M能使湿润的红色石蕊试纸变蓝.Z是人体血红蛋白中存在的金属元素.请填写下列空白: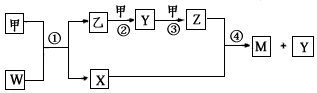
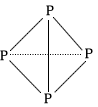 ,请画出C4A44+(每个原子最外层均达到 稳定结构)的结构式:___(A、C用元素符号表示)。
,请画出C4A44+(每个原子最外层均达到 稳定结构)的结构式:___(A、C用元素符号表示)。