题目内容
【题目】某温度下,C和H2O(g)在密闭容器里发生下列反应:
①C(s)+H2O(g)![]() CO(g)+H2(g), ②CO(g)+H2O(g)
CO(g)+H2(g), ②CO(g)+H2O(g)![]() CO2(g)+H2(g)
CO2(g)+H2(g)
当反应达到平衡时,c(H2)=1.9 mol·L-1,c(CO)=0.1 mol·L-1。则下列叙述正确的有
A.CO在平衡时转化率为10%
B.平衡浓度c(CO2)=c(H2)
C.平衡时气体平均相对分子质量约为23.3
D.其他条件不变时,缩小体积,H2O(g)的转化率随之降低
【答案】D
【解析】
试题分析:C(s)+H2O(g)===CO(g)+H2(g) 假设①生成xmolCO,那么同时生成xmolH2,xmolCO继续跟水发生第②反应,其中有ymol参加了实际反应,所以CO(g)+H2O(g)===CO2(g)+H2(g) 假设该容器为1L,那么最后有H2为1.9mol,CO只有0.1mol,所以 x-y=0.1(CO的量) x+y=1.9 (H2的量) 解得x=1,y=0.9,也就是第一步产生了1molCO和1molH2,第二步有0.9molCO参加反应,生成0.9molCO2 和0.9molH2。A. CO的转化率为 0.9/1=90%,错误;B.平衡时CO2浓度为0.9/1=0.9mol/L,而氢气是c(H2)=1.9mol/L,不相等,错误;C.平衡时,有0.1molCO,0.9molCO2, 1.9molH2, 平均相对分子质量为(2.8+39.6+3.8)÷2.9 =15.93,错误。D.其他条件不变时,缩小体积,①平衡逆向移动,②平衡不移动,所以H2O(g)的转化率随之降低,正确。

【题目】甲醇既是重要的化工原料,又可作为燃料,还可以作为燃料电池的原料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g) ![]() CH3OH(g) ΔH1 (已知:CO的结构与N2相似)
CH3OH(g) ΔH1 (已知:CO的结构与N2相似)
②CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g)ΔH2
CH3OH(g)+H2O(g)ΔH2
③CO2(g)+H2(g) ![]() CO(g)+H2O(g) ΔH3
CO(g)+H2O(g) ΔH3
回答下列问题:
(1)已知反应①中相关的化学键键能数据如下:
化学键 | H-H | C-O | C=O | H-O | C-H |
E/(KJ/mol) | 436 | 343 | 1076 | 465 | 413 |
由此计算ΔH1=______kJ·mol-1,已知ΔH2=-58kJ·mol-1,则ΔH3=_____kJ·mol-1。
(2)已知:
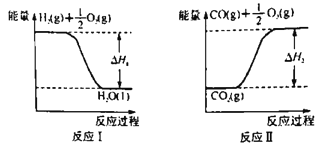
若甲醇的燃烧热为ΔH3,试用ΔH1、ΔH2、ΔH3表示CO(g)+2H2(g) ![]() CH3OH(l)的ΔH=________。若ΔH1=-285.8 kJ·mol-1,ΔH2=+283.0 kJ·mol-1,某H2和CO的混合气体完全燃烧时放出113.74 kJ热量,同时生成3.6g液态水,则原混合气体中H2和CO的物质的量之比为______。
CH3OH(l)的ΔH=________。若ΔH1=-285.8 kJ·mol-1,ΔH2=+283.0 kJ·mol-1,某H2和CO的混合气体完全燃烧时放出113.74 kJ热量,同时生成3.6g液态水,则原混合气体中H2和CO的物质的量之比为______。
(3)以CH4和H2O为原料,通过下列反应也可以制备甲醇。
Ⅰ:CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH=+206.0 kJ·mol-1
Ⅱ:CO(g)+2H2(g)= =CH3OH (g)ΔH=-129.0 kJ·mol-1
CH4(g)+H2O(g)反应生成CH3OH(g)和H2(g)的热化学方程式为__________.