题目内容
9.下列物质的系统命名中,错误的是( )| A. |  2,4-二甲基己烷 2,4-二甲基己烷 | |
| B. |  2-甲基-4-戊炔 2-甲基-4-戊炔 | |
| C. |  3-甲基-2-丁醇 3-甲基-2-丁醇 | |
| D. | CH3-CHBr-CHBr-CH3 2,3-二溴丁烷 |
分析 A、烷烃命名符合:长、多、近、小、简原则;
B、炔烃命名选取含有碳碳三键额的最长碳链,距离三键最近得到一端为1号碳;
C、醇类命名选取含有羟基的最长碳链,据此羟基最近的一端命名为1号碳;
D、氯代烃命名选取含有最多卤素原子的最长碳链.
解答 解:A、 最长碳链为6,在2、4号碳上分别含有1个甲基,命名为:2,4-二甲基己烷,故A正确;
最长碳链为6,在2、4号碳上分别含有1个甲基,命名为:2,4-二甲基己烷,故A正确;
B、 含有三键的最长碳链为5,在4号碳上含有1个甲基,命名为:4-甲基-1-戊炔,故B错误;
含有三键的最长碳链为5,在4号碳上含有1个甲基,命名为:4-甲基-1-戊炔,故B错误;
C、 含有羟基的最长碳链为4,在3号碳上含有1个甲基,命名为:3-甲基-2-丁醇,故C正确;
含有羟基的最长碳链为4,在3号碳上含有1个甲基,命名为:3-甲基-2-丁醇,故C正确;
D、CH3-CHBr-CHBr-CH3 含有2个Br原子的最长碳链为4,正确命名为:2,3-二溴丁烷,故D正确,
故选B.
点评 本题主要考查的是常见有机化合物的命名,涉及烷烃命名、醇类命名、炔烃命名以及卤代烃的命名,难度不大.

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
17.关于浓H2SO4、稀H2SO4的叙述中正确的是( )
| A. | 浓H2SO4、稀H2SO4都难挥发 | |
| B. | 浓H2SO4、稀H2SO4都有氧化性,故浓H2SO4、稀H2SO4都是氧化性的酸 | |
| C. | 浓H2SO4、稀H2SO4在加热时都能与铜反应 | |
| D. | 浓H2SO4、稀H2SO4在常温下都能用铁制容器贮存 |
4.A、B、C、D、E是中学化学中五种常见元素,有关信息如下:
请回答下列问题:
(1)A的氢化物分子式是NH3,用电子式表示该物质的形成过程为: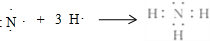 .写出实验室制取该物质的化学方程式Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.
.写出实验室制取该物质的化学方程式Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.
(2)A、D的氢化物相互反应,产生白色固体,对该固体中阳离子存在检验的操作方法是:取该白色固体少许于试管中,加入适量浓NaOH溶液并加热,用湿润的红色石蕊试纸接近试管口检验放出的气体,若试纸变蓝(或用蘸有浓盐酸的玻璃棒靠近试管口,有白烟产生).
(3)A与B可组成质量比为7:16的三原子分子,该分子释放在空气中其化学作用可能引发的后果有:①③ ①酸雨 ②温室效应 ③光化学烟雾 ④臭氧层破坏.
| 元素 | 有关信息 |
| A | 其氢化物水溶液呈碱性 |
| B | 地壳中含量最多的元素 |
| C | 单质须保存在煤油中 |
| D | 单质与NaOH溶液反应可用于生产漂白液 |
| E | 单质是生活中用量最大的金属,其制品在潮湿空气中易被腐蚀或损坏 |
(1)A的氢化物分子式是NH3,用电子式表示该物质的形成过程为:
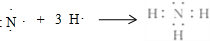 .写出实验室制取该物质的化学方程式Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.
.写出实验室制取该物质的化学方程式Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.(2)A、D的氢化物相互反应,产生白色固体,对该固体中阳离子存在检验的操作方法是:取该白色固体少许于试管中,加入适量浓NaOH溶液并加热,用湿润的红色石蕊试纸接近试管口检验放出的气体,若试纸变蓝(或用蘸有浓盐酸的玻璃棒靠近试管口,有白烟产生).
(3)A与B可组成质量比为7:16的三原子分子,该分子释放在空气中其化学作用可能引发的后果有:①③ ①酸雨 ②温室效应 ③光化学烟雾 ④臭氧层破坏.
1.环癸五烯的结构简式可表示为 ,下列说法正确的是( )
,下列说法正确的是( )
 ,下列说法正确的是( )
,下列说法正确的是( )| A. | 根据 的结构特点可知环癸五烯的分子式为C10H8 的结构特点可知环癸五烯的分子式为C10H8 | |
| B. | 常温常压下环癸五烯是一种易溶于水的无色气体 | |
| C. | 环癸五烯既能使溴水褪色,又能使酸性KMnO4溶液褪色 | |
| D. | 乙烯和环癸五烯互为同系物 |
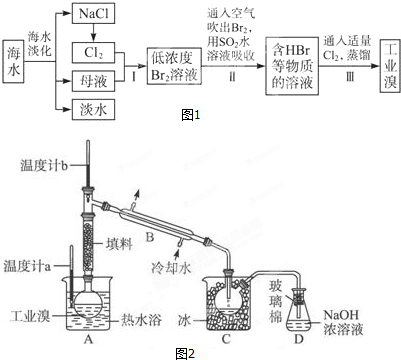

 的名称是3-甲基-1-丁醇
的名称是3-甲基-1-丁醇