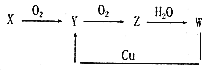题目内容
【题目】如图是某煤发电厂处理废气的装置示意图。下列说法错误的是( )
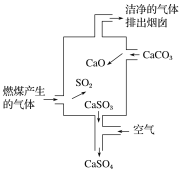
A.使用此废气处理装置可减少酸雨的形成
B.装置内发生的反应有化合、分解、置换和氧化还原反应
C.整个过程的反应可表示为2SO2+2CaCO3+O2===2CaSO4+2CO2
D.可用酸性高锰酸钾溶液检验废气处理是否达标
【答案】B
【解析】
A、二氧化硫是形成酸雨的重要物质,经过处理后能减少酸雨的形成,故A正确;
B、碳酸钙受热生成氧化钙和二氧化碳的反应属于分解反应;二氧化硫与石灰水反应生成CaSO3和CaSO4是中和反应、化合反应,氧化还原反应,但没有置换反应,故B错误;
C、整个过程中,二氧化硫与碳酸钙和氧气反应生成了硫酸钙和二氧化碳,化学反应式可表示为2SO2+2CaCO3+O2=2CaSO4+2CO2,故C正确;
D、二氧化硫具有还原性,易被高锰酸钾溶液氧化反应使高锰酸钾溶液褪色,可用酸性高锰酸钾溶液检验废气处理是否达标,故D正确;
故选B。

【题目】—定温度下,向10mL0.40mol/LH2O2 溶液中加入少量FeCl3溶液(忽略整个过程中溶液体积的变化),不同时刻测得生成O2的体积(已折算为标准状况下)如表所示:
t/min | 0 | 2 | 4 | 6 |
V(O2)/mL | 0 | 9.9 | 17.5 | 22.4 |
资料显示,反应分两步进行:①2Fe3++H2O2=2Fe2++2H++O2;②H2O2+2Fe2++2H+=2H2O+2Fe3+。反应过程中能量变化如图所示。下列说法正确的是
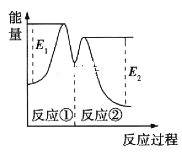
A. Fe2+的作用是增大过氧化氢的分解速率
B. 反应①、②均是放热反应
C. 反应2H2O2(aq)=2H2O(l)+O2(g)是吸热反应
D. 0~6min内的平均反应速率v(H2O2)=3.33×10-2mol/(L·min)
【题目】汽车尾气中含有CO、NO等有害气体。
(1)通过NO传感器可监测汽车尾气中NO的含量其工作原理如图所示。已知:![]() 可在固体电解质中自由移动。
可在固体电解质中自由移动。
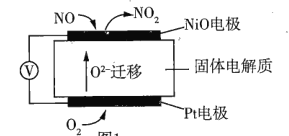
①NO电极上发生的是______(填“氧化”或“还原”)反应。
②外电路中,电子是从______(填“NO”或Pt”)电极流出。
③Pt电极上的电极反应式为______。
(2)一种新型催化剂用于NO和CO的反应:![]() 。已知增大催化剂的比表面积可提高该反应的速率,为了验证温度、催化剂的比表面积对化学反应速率的影响,某同学设计了三组实验,如表所示。
。已知增大催化剂的比表面积可提高该反应的速率,为了验证温度、催化剂的比表面积对化学反应速率的影响,某同学设计了三组实验,如表所示。
实验编号 |
| NO初始浓度/( | CO初始浓度/( | 催化剂的比表面积( |
Ⅰ | 280 |
|
| 82 |
Ⅱ | 280 |
|
| 124 |
Ⅲ | 350 | a |
| 82 |
①表中a=______。
②能验证温度对化学反应速率影响的是实验______(填实验序号)。
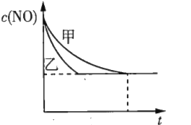
③实验I和实验Ⅱ中,NO的物质的量浓度![]() 随时间t的变化曲线如图所示,其中表示实验Ⅱ的是曲线______(填“甲”或“乙”)。
随时间t的变化曲线如图所示,其中表示实验Ⅱ的是曲线______(填“甲”或“乙”)。
(3)在容积固定的绝热容器中发生反应![]() ,不能说明该反应已达到平衡状态的是______(填序号)。
,不能说明该反应已达到平衡状态的是______(填序号)。
A.容器内温度不再变化 B.容器内的气体压强保持不变
C.![]() D.容器内混合气体的密度保持不变
D.容器内混合气体的密度保持不变