题目内容
常温时,下列叙述正确的是
A.pH=9的NH4Cl与NH3·H2O混合溶液中c(Cl-)>c(NH4+)
B.pH=2.5的可乐中c(H+)是pH=3.5的柠檬水中c(H+)的1 0倍
C.AgCl在0.1 mol/L CaCl2溶液和0.l mol/L NaCl溶液中的溶解度相同
D.1 mL l mol l L Na2CO3溶液加水稀释至100 mL,pH和Kw均减小
B
【解析】
试题分析:A、pH=9的NH4Cl与NH3·H2O混合溶液中NH3·H2O的电离程度大于NH4Cl的水解程度,所以c(Cl-)<c(NH4+),错误;B、pH=2.5的可乐中c(H+)=1×10-2.5mol/L,pH=3.5的柠檬水中c(H+)=1×10-3.5mol/L,前者是后者的10倍,正确;C、0.1 mol/L CaCl2溶液和0.l mol/L NaCl溶液中的氯离子的浓度不同,导致AgCl的溶解度不同,错误;D、Kw是温度常数,温度不变,Kw不变,错误,答案选B。
考点:考查混合液的离子浓度的比较,pH的计算,溶液稀释过程中pH和Kw的判断,同一物质在不同溶剂中的溶解度的判断

 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案(14分)甲学生对Cl2与FeCl2和KSCN混合溶液的反应进行实验探究。
操 作 | 现 象 |
通入氯气至过量
| I.A中溶液变红 II.稍后,溶液由红色变为黄色
|
(1)B中反应的离子方程式是______。
(2)A中溶液变红的原因是______。
(3)为了探究现象II的原因,甲同学进行如下实验。
①取A中黄色溶液于试管中,加入NaOH溶液,有红褐色沉淀生成,则溶液中一定存在_______。
②取A中黄色溶液于试管中,加入过量的KSCN溶液,最终得到红色溶液。
甲同学的实验证明产生现象II的原因是SCN—与Cl2发生了反应。
(4)甲同学猜想SCN—可能被Cl2氧化了,他又进行了如下研究。
资料显示:SCN—的电子式为 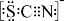 。
。
①甲同学认为SCN—中碳元素没有被氧化,理由是______。
②取A中黄色溶液于试管中,加入用盐酸酸化的BaCl2溶液,产生白色沉淀,由此证明SCN—中被氧化的元素是______。
③通过实验证明了SCN—中氮元素转化为,他的实验方案是______。
④若SCN—与Cl2反应生成1 mol CO2,则转移电子的物质的量是______mol。





 (1)若用CmHn表示汽油的主要组成,CmHn在空气中完全燃烧的化学方程式为 ,汽油燃烧产生能量为汽车提供了动力,这一过程中能量的转化是由 能转化为 能,最终转化为机械能;
(1)若用CmHn表示汽油的主要组成,CmHn在空气中完全燃烧的化学方程式为 ,汽油燃烧产生能量为汽车提供了动力,这一过程中能量的转化是由 能转化为 能,最终转化为机械能;