题目内容
【题目】氮及其化合物在工农业生产生活中应用广泛,请解决下列问题.
(1)化合物甲(由氮和另一种常见的主族元素组成)是一种新型无机材料.将8.2g甲溶于足量的氢氧化钠溶液,可产生标准状况下为4.48L的气体,该气体可作制冷剂.向反应后的溶滚中逐滴加入稀盐酸,产生白色沉淀质量最大为15.6g,继续滴加沉淀消失.则甲溶于氢氧化钠的化学方程式为 .
(2)NH3催化还原氮氧化物是目前应用广泛的烟气氮氧化物脱除技术.例如:
4NH3(g)+6NO(g)5N2(g)+6H2O(g)△H1
己知:①H2O(l)=H2O(g)△H2
②4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H3
则NH3(g)的标准燃烧热△H= .
以FeSO4作催化剂在不同温度下,经过相同的时间测试氨还原氮氧化物效果如图1,当反应在400~450℃,NOx的转化率随温度升高而降低.当体系温度升至500℃以上时.NOx的转化率迅速下降,其可能原因是 . 图2反映的是在400℃N2的体积分数与反应物中 ![]() 的关系,请在下面的图2上画出450℃的变化趋势曲线 .
的关系,请在下面的图2上画出450℃的变化趋势曲线 .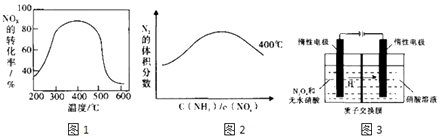
(3)N2O5是绿色硝化试剂,溶于水可得硝酸.图3是以N2O4为原料电解制备N2O5的装置示意图.写出阳极区生成N2O5的电极反应式是 .
(4)常温下,向0.1mol/L氨水中加入少许N2O5 , 使溶液中c(NH3H2O):c(NH4+)=5:9,此时溶液的pH= . (25℃时.NH3H2O的电离平衡常数Kb=1.8×10﹣5)
【答案】
(1)AlN+NaOH+H2O=NaAlO2+NH3↑
(2)![]() ;催化剂活性降低(FeSO4受热分解);
;催化剂活性降低(FeSO4受热分解);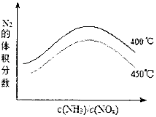
(3)N2O4﹣2e﹣+2HNO3=2N2O5+2H+
(4)9
【解析】解:(1)化合物甲(由氮和另一种常见的主族元素组成),溶于足量的氢氧化钠溶液,产生的气体可作制冷剂为氨气,产生标准状况下为4.48L的气体,n(NH3)= ![]() =0.2mol,反应后的溶滚中逐滴加入稀盐酸,先沉淀后沉淀为溶解,为铝的化合物的特征,产生白色沉淀质量最大为15.6g,为氢氧化铝,n[Al(OH)3]=
=0.2mol,反应后的溶滚中逐滴加入稀盐酸,先沉淀后沉淀为溶解,为铝的化合物的特征,产生白色沉淀质量最大为15.6g,为氢氧化铝,n[Al(OH)3]= ![]() =0.2mol,则m(N)+m(Al)=0.2mol×14g/mol+0.2mol×27g/mol=8.2g,则8.2g甲为AlN,甲溶于氢氧化钠的化学方程式为AlN+NaOH+H2O=NaAlO2+NH3↑,
=0.2mol,则m(N)+m(Al)=0.2mol×14g/mol+0.2mol×27g/mol=8.2g,则8.2g甲为AlN,甲溶于氢氧化钠的化学方程式为AlN+NaOH+H2O=NaAlO2+NH3↑,
所以答案是:AlN+NaOH+H2O=NaAlO2+NH3↑;(2)氨气燃烧生成氮气和水,①4NH3(g)+6NO(g)5N2(g)+6H2O(g)△H1②H2O(l)=H2O(g)△H2 ③4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H3根据盖斯定律,将已知热化学方程式 ![]() (③×3+①×2﹣②×30)得:4NH3(g)+3O2(g)=2N2(g)+6H2O(l)△H=
(③×3+①×2﹣②×30)得:4NH3(g)+3O2(g)=2N2(g)+6H2O(l)△H= ![]() ;当反应在400~450℃,NOx的转化率随温度升高而降低.当体系温度升至500℃以上时,催化剂硫酸亚铁受热分解,催化剂活性降低,所以450℃的变化趋势曲线图为:
;当反应在400~450℃,NOx的转化率随温度升高而降低.当体系温度升至500℃以上时,催化剂硫酸亚铁受热分解,催化剂活性降低,所以450℃的变化趋势曲线图为:  ,
,
所以答案是: ![]() ;催化剂活性降低(FeSO4受热分解);
;催化剂活性降低(FeSO4受热分解);  ;(3)NO2可电解制备绿色硝化试剂N2O5 . N元素化合价升高,NO2被氧化,电极方程式为N2O4﹣2e﹣+2HNO3=2N2O5+2H+ ,
;(3)NO2可电解制备绿色硝化试剂N2O5 . N元素化合价升高,NO2被氧化,电极方程式为N2O4﹣2e﹣+2HNO3=2N2O5+2H+ ,
所以答案是:N2O4﹣2e﹣+2HNO3=2N2O5+2H+;(4)常温下,向0.1mol/L氨水中加入少许N2O5 , 五氧化二氮和水反应生成硝酸,硝酸和氨水反应,溶液中c(NH3H2O):c(NH4+)=5:9,溶液中溶质为硝酸铵和一水合氨,NH3H2ONH4++OH﹣ , 25℃时.NH3H2O的电离平衡常数Kb=1.8×10﹣5= 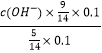 ,c(OH﹣)=10﹣5mol/L,c(H+)=10﹣9mol/L,PH=9,
,c(OH﹣)=10﹣5mol/L,c(H+)=10﹣9mol/L,PH=9,
所以答案是:9.
【考点精析】解答此题的关键在于理解化学平衡状态本质及特征的相关知识,掌握化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效),以及对弱电解质在水溶液中的电离平衡的理解,了解当弱电解质分子离解成离子的速率等于结合成分子的速率时,弱电解质的电离就处于电离平衡状态;电离平衡是化学平衡的一种,同样具有化学平衡的特征.条件改变时平衡移动的规律符合勒沙特列原理.