题目内容
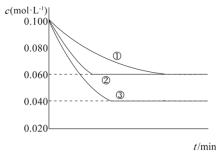
【题目】在溶液中,反应A+2B![]() C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)=0.100mol·L-1、c(B)=0.200mol·L-1及c(C)=0mol·L-1,反应物A的浓度随时间的变化如图所示。下列说法不正确的是
C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)=0.100mol·L-1、c(B)=0.200mol·L-1及c(C)=0mol·L-1,反应物A的浓度随时间的变化如图所示。下列说法不正确的是
A.与①比较,②可能加入催化剂
B.与①比较,③可能是增大了压强
C.实验②平衡时B的转化率为40%
D.该反应的ΔH﹥0
【答案】D
【解析】
题中提供的是A浓度随时间变化的图像,根据反应速率的表达式,图像中浓度变化越快表明反应速率越大;最终平衡时,若两个体系的A的浓度相等,则表明两个体系平衡组成相同;A的平衡浓度越小,表明反应整体向右进行的更彻底。
A.由图可知,②相比于①反应速率更大,但平衡时组成都相同;加入催化剂能够提高反应速率,但不会影响平衡,A项正确;
B.由图可知,③相比于①,反应速率更快,并且反应向右进行的更彻底;加压可以提高反应速率,也可以让平衡正向移动,反应进行更彻底,B项正确;
C.由图可知,②达到平衡时,A的浓度下降了0.04mol/L,那么B的浓度就下降0.08mol/L,由转化率的定义计算可知,B的转化率为40%,C项正确;
D.由题干的信息无法判断反应是吸热还是放热的,D项错误;
答案选D。

【题目】一定温度下,在3个体积均为1.0L的恒容密闭容器中反应2H2(g)+CO(g)![]() CH3OH(g)达到平衡。下列说法正确的是( )
CH3OH(g)达到平衡。下列说法正确的是( )
容器 | 温度/K | 物质的起始浓度mol·L-1 | 物质的平衡浓度/mol·L-1 | ||
c(H2) | c(CO) | c(CH3OH) | c(CH3OH) | ||
Ⅰ | 400 | 0.20 | 0.10 | 0 | 0.080 |
Ⅱ | 400 | 0.40 | 0.20 | 0 | |
Ⅲ | 500 | 0 | 0 | 0.10 | 0.025 |
A.该反应的正反应放热
B.达到平衡时,容器Ⅰ中反应物转化率比容器Ⅱ中的大
C.达到平衡时,容器Ⅱ中c(H2)大于容器Ⅲ中c(H2)的两倍
D.达到平衡时,容器Ⅲ中的正反应速率比容器Ⅰ中的小