题目内容
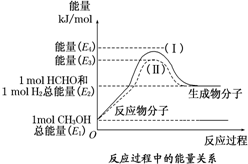 甲醛是一种重要的化工产品,可利用甲醇催化脱氢制备.甲醛与气态甲醇转化的能量关系如图所示.
甲醛是一种重要的化工产品,可利用甲醇催化脱氢制备.甲醛与气态甲醇转化的能量关系如图所示.(1)甲醇催化脱氢转化为甲醛的反应是
(2)过程Ⅰ与过程Ⅱ的反应热是否相同?
(3)写出甲醇催化脱氢转化为甲醛的热化学方程
(4)甲醇催化脱氢转化为甲醛的过程中,如果要使反应温度维持在700℃,需向体系中通入空气,则进料甲醇与空气的物质的量理论比值为
| 1 |
| 2 |
| ||
考点:热化学方程式,吸热反应和放热反应
专题:
分析:(1)通过比较反应物和生成物的总能量的角度来得出反应吸放热;
(2)反应热取决于反应物和生成物的总能量的大小,与起始状态和反应的最终状态有关,而与反应的途径无关;
(3)根据图象得出反应热的数值,根据热化学方程式的书写方法写出;
(4)要使反应维持在一定温度持续进行,应保证反应H2(g)+
O2(g)=H2O(g)△H2=-akJ?mol-1
放出的热量恰好被反应CH30H(g)=CH20(g)+H2(g)△H1=(E2-E1)kJ?mol-1全部利用.因此根据反应方程式的关系可知:甲醇与氧气的物质的量之比为
,根据空气中氧气的体积分数0.2,可求得甲醇与空气的物质的量之比,据此即可解答.
(2)反应热取决于反应物和生成物的总能量的大小,与起始状态和反应的最终状态有关,而与反应的途径无关;
(3)根据图象得出反应热的数值,根据热化学方程式的书写方法写出;
(4)要使反应维持在一定温度持续进行,应保证反应H2(g)+
| 1 |
| 2 |
放出的热量恰好被反应CH30H(g)=CH20(g)+H2(g)△H1=(E2-E1)kJ?mol-1全部利用.因此根据反应方程式的关系可知:甲醇与氧气的物质的量之比为
| 2a |
| E2-E1 |
解答:
解:(1)通过图象可以看出,反应物的总能量比生成物的总能量低,故为吸热反应,故答案为:吸热.
(2)一个化学反应的热效应仅与反应的起始状态和反应的最终状态有关,与反应的途径无关,仅取决于反应物和生成物的总能量的大小,过程Ⅰ与过程Ⅱ的反应热是相同的,故答案为:相同 一个化学反应的反应热仅与反应的起始状态和反应的最终状态有关,而与反应的途径无关.
(3)从图象可以看出,甲醇催化脱氢转化为甲醛为吸热反应,而且吸收热量为(E2-E1),故热化学方程式为:
CH3OH(g)
HCHO(g)+H2(g)△H=(E2-E1) kJ/mol,故答案为:CH3OH(g)
HCHO(g)+H2(g)△H=(E2-E1) kJ/mol
(4)反应维持在一定温度持续进行,应保证反应H2(g)+
O2(g)=H2O(g)△H2=-akJ?mol-1
放出的热量恰好被反应CH30H(g)=CH20(g)+H2(g)△H1=(E2-E1)kJ?mol-1全部利用.即CH30H反应吸收的热量等于氢气燃烧放出的热量,设需甲醇的物质的量为n(CH30H),需氧气的物质的量为n(O2),则有:n(CH30H)×(E2-E1)=n(O2)×2×a,解得:
甲醇与氧气的物质的量之比
=
,根据空气中氧气的体积分数0.2,即可得出
=
,故答案为:
(2)一个化学反应的热效应仅与反应的起始状态和反应的最终状态有关,与反应的途径无关,仅取决于反应物和生成物的总能量的大小,过程Ⅰ与过程Ⅱ的反应热是相同的,故答案为:相同 一个化学反应的反应热仅与反应的起始状态和反应的最终状态有关,而与反应的途径无关.
(3)从图象可以看出,甲醇催化脱氢转化为甲醛为吸热反应,而且吸收热量为(E2-E1),故热化学方程式为:
CH3OH(g)
| 催化剂 |
| 催化剂 |
(4)反应维持在一定温度持续进行,应保证反应H2(g)+
| 1 |
| 2 |
放出的热量恰好被反应CH30H(g)=CH20(g)+H2(g)△H1=(E2-E1)kJ?mol-1全部利用.即CH30H反应吸收的热量等于氢气燃烧放出的热量,设需甲醇的物质的量为n(CH30H),需氧气的物质的量为n(O2),则有:n(CH30H)×(E2-E1)=n(O2)×2×a,解得:
甲醇与氧气的物质的量之比
| n(CH30H) |
| n(O2) |
| 2a |
| E2-E1 |
| n(CH30H) |
| n(O2) |
| 2a |
| 5(E2-E1) |
| 2a |
| 5(E2-E1) |
点评:本题主要考查了热化学方程式的书写和反应热的计算,理清甲醇和氢气的热量关系是解答本题的关键,题目难度中等.

练习册系列答案
 走进文言文系列答案
走进文言文系列答案
相关题目
将NH4NO3加热反应,有N2、HNO3和H2O生成,配平后的方程式中计量系数由小到大的顺序是( )
| A、NH4NO3、N2、HNO3、H2O |
| B、HNO3、N2、NH4NO3、H2O |
| C、H2O、NH4NO3、N2、HNO3 |
| D、N2、NH4NO3、HNO3、H2O |
下列四种物质中,既能与水发生反应,又能与碱发生反应的是( )
| A、Cl2 |
| B、CO2 |
| C、NO |
| D、SiO2 |
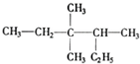
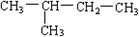 ⑧
⑧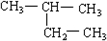
 ?2,2-二甲基丁烷.
?2,2-二甲基丁烷.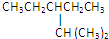
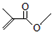 的分子式:
的分子式: